
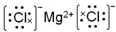 £®
£®
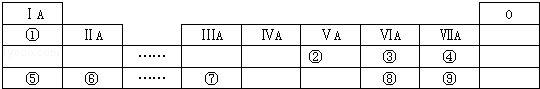
·ÖĪö ÓɶĢÖÜĘŚŌŖĖŲŌŚÖÜĘŚ±ķµÄĪ»ÖĆæÉÖŖ£¬¢Ł”«¢į·Ö±šŹĒH”¢N”¢O”¢F”¢Na”¢Mg”¢Al”¢S”¢Cl£¬
£Ø1£©·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦Ēā»ÆĪļŌ½ĪČ¶Ø£»
£Ø2£©ŌŖĖŲ¢ŻŗĶ¢ßµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ·¢Éś·“Ó¦£¬Éś³ÉĘ«ĀĮĖįÄĘŗĶĒāĘų£»
£Ø3£©ŌŖĖŲ¢ŽŗĶ¢įŠĪ³ÉµÄ»ÆŗĻĪļĪŖĀČ»ÆĆ¾£¬ĪŖĄė×Ó»ÆŗĻĪļ£»
£Ø4£©¾ßÓŠĻąĶ¬µē×Ó²ć½į¹¹µÄĄė×Ó£¬Ō×ÓŠņŹż“óµÄĄė×Ó°ė¾¶Š”£»
£Ø5£©Ēā»ÆĪļAŗĶB¶¼ŗ¬ÓŠ18øöµē×Ó£¬AŹĒŅ»ÖÖ6Ō×Ó·Ö×Ó£¬æÉ×ö»š¼ż·¢¶Æ»śČ¼ĮĻ£»BŹĒŅ»ÖÖ³£¼ūĒæŃõ»Æ¼Į£®ŅŃÖŖŅŗĢ¬AÓėŅŗĢ¬B³ä·Ö·“Ӧɜ³ÉŅ»ÖÖŅŗĢ¬10µē×Ó·Ö×ÓŗĶŅ»ÖÖĘųĢ¬µ„ÖŹ£¬æÉÖŖ¹żŃõ»ÆĒāÓėN2H4·“Ӧɜ³ÉµŖĘųŗĶĖ®£»
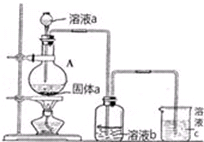
£Ø6£©±Č½ĻŌŖĖŲ¢ąŗĶ¢į·Ē½šŹōŠŌµÄĻą¶ŌĒæČõ£¬ĄūÓƵ„ÖŹÖ®¼äµÄÖĆ»»·“Ó¦æÉÖ¤Ć÷£¬ŌņČÜŅŗaĪŖÅØŃĪĖį£¬¹ĢĢåaĪŖ¶žŃõ»ÆĆĢ£¬ČÜŅŗbĪŖNa2S£Ø»ņH2S£©£¬ČÜŅŗbÖŠÉś³É³ĮµķæÉĖµĆ÷·Ē½šŹōŠŌ£¬×īŗóÉÕ±ÖŠNaOHČÜŅŗĪüŹÕĪ²Ęų£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗÓɶĢÖÜĘŚŌŖĖŲŌŚÖÜĘŚ±ķµÄĪ»ÖĆæÉÖŖ£¬¢Ł”«¢į·Ö±šŹĒH”¢N”¢O”¢F”¢Na”¢Mg”¢Al”¢S”¢Cl£¬
£Ø1£©·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦Ēā»ÆĪļŌ½ĪČ¶Ø£¬ŌņŌŖĖŲ¢Ū¢Ü¢ąµÄĘųĢ¬Ēā»ÆĪļÖŠ×īĪČ¶ØµÄŹĒHF£¬¹Ź“š°øĪŖ£ŗHF£»
£Ø2£©ŌŖĖŲ¢ŻŗĶ¢ßµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ·¢Éś·“Ó¦£¬Éś³ÉĘ«ĀĮĖįÄĘŗĶĒāĘų£¬Ąė×Ó·“Ó¦ĪŖAl£ØOH£©3+OH-=AlO2-+2H2O£¬¹Ź“š°øĪŖ£ŗAl£ØOH£©3+OH-=AlO2-+2H2O£»
£Ø3£©ŌŖĖŲ¢ŽŗĶ¢įŠĪ³ÉµÄ»ÆŗĻĪļĪŖĀČ»ÆĆ¾£¬ĪŖĄė×Ó»ÆŗĻĪļ£¬µē×ÓŹ½ĪŖ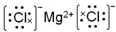 £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ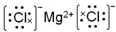 £»
£»
£Ø4£©¾ßÓŠĻąĶ¬µē×Ó²ć½į¹¹µÄĄė×Ó£¬Ō×ÓŠņŹż“óµÄĄė×Ó°ė¾¶Š”£¬¢Ū”¢¢Ż”¢¢ŽŠĪ³ÉµÄ¼ņµ„Ąė×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņĪŖO2-£¾Na+£¾Mg2+£¬¹Ź“š°øĪŖ£ŗO2-£¾Na+£¾Mg2+£»
£Ø5£©Ēā»ÆĪļAŗĶB¶¼ŗ¬ÓŠ18øöµē×Ó£¬AŹĒŅ»ÖÖ6Ō×Ó·Ö×Ó£¬æÉ×ö»š¼ż·¢¶Æ»śČ¼ĮĻ£»BŹĒŅ»ÖÖ³£¼ūĒæŃõ»Æ¼Į£®ŅŃÖŖŅŗĢ¬AÓėŅŗĢ¬B³ä·Ö·“Ӧɜ³ÉŅ»ÖÖŅŗĢ¬10µē×Ó·Ö×ÓŗĶŅ»ÖÖĘųĢ¬µ„ÖŹ£¬æÉÖŖ¹żŃõ»ÆĒāÓėN2H4·“Ӧɜ³ÉµŖĘųŗĶĖ®£¬·“Ó¦ĪŖN2H4+2H2O2=N2+4H2O£¬¹Ź“š°øĪŖ£ŗN2H4+2H2O2=N2+4H2O£»
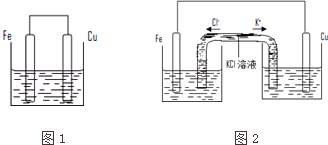
£Ø6£©±Č½ĻŌŖĖŲ¢ąŗĶ¢į·Ē½šŹōŠŌµÄĻą¶ŌĒæČõ£¬ĄūÓƵ„ÖŹÖ®¼äµÄÖĆ»»·“Ó¦æÉÖ¤Ć÷£¬ŌņČÜŅŗaĪŖÅØŃĪĖį£¬¹ĢĢåaĪŖ¶žŃõ»ÆĆĢ£¬ČÜŅŗbĪŖNa2S£Ø»ņH2S£©£¬ČÜŅŗbÖŠÉś³É³ĮµķæÉĖµĆ÷·Ē½šŹōŠŌ£¬×īŗóÉÕ±ÖŠNaOHČÜŅŗĪüŹÕĪ²Ęų£¬
¢ŁÓÉÉĻŹö·ÖĪö£¬ÅØČÜŅŗaŗĶČÜŅŗb·Ö±šĪŖÅØHCl”¢Na2S£Ø»ņH2S£©£¬¹Ź“š°øĪŖ£ŗÅØHCl£»Na2S£Ø»ņH2S£©£»
¢ŚÅØČÜŅŗaÓėŗŚÉ«¹ĢĢåa·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖMnO2+4H++2Cl-$\frac{\underline{\;\;”÷\;\;}}{\;}$Mn2++Cl2”ü+2H2O£¬¹Ź“š°øĪŖ£ŗMnO2+4H++2Cl-$\frac{\underline{\;\;”÷\;\;}}{\;}$Mn2++Cl2”ü+2H2O£®
µćĘĄ ±¾Ģāæ¼²éĪ»ÖĆ”¢½į¹¹ÓėŠŌÖŹµÄ¹ŲĻµ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŌŖĖŲµÄĪ»ÖĆ”¢ŠŌÖŹ”¢ŌŖĖŲÖÜĘŚĀÉ”¢ŌŖĖŲ»ÆŗĻĪļÖŖŹ¶ĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅā£Ø6£©ÖŠ·Ē½šŹōŠŌ±Č½Ļ¼°ŹµŃéÉč¼ĘµÄÄÜĮ¦£¬ĢāÄæÄŃ¶Č²»“ó£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĞĻÄĪĄŅ»øßŅ»ÉĻ10ŌĀŌĀæ¼»Æѧb¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ¼ĘĖćĢā
ĻÖÓŠ4gĒāŃõ»ÆÄĘĒ”ŗĆÓė100mlµÄŃĪĖįĶźČ«·“Ó¦£¬ŹŌ¼ĘĖć(Š“¼ĘĖć¹ż³Ģ)
£Ø1£©ĒāŃõ»ÆÄʵÄĪļÖŹµÄĮæ
£Ø2£©ŃĪĖįµÄĪļÖŹµÄĮæÅضČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĮÉÄžŹ”øßŅ»ÉĻ10ŌĀŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃé²Ł×÷ÕżČ·µÄŹĒ
A. µ±Ä³ŹµŃéĆ»ÓŠ×¼Č·µÄŅ©Ę·ÓĆĮæĖµĆ÷Ź±£¬ĪŖ擵½Ć÷ĻŌĻÖĻó£¬Č”ÓĆŅ©Ę·Ō½¶ąŌ½ŗĆ
B. Č”ÓĆĻøæŚĘæĄļµÄŹŌŅŗŹ±£¬ĻČÄĆĻĀĘæČū£¬µ¹·ÅŌŚ×ĄÉĻ£¬Č»ŗó±źĒ©³ÆĶāÄĆĘšĘæ×Ó£¬ĘææŚŅŖ½ō°¤×ÅŹŌ¹ÜæŚ£¬½«ŅŗĢå»ŗ»ŗµŲµ¹ČėŹŌ¹Ü
C. ½ŗĶ·µĪ¹ÜČ”ĶźŅ»ÖÖŹŌŅŗŗó£¬æÉÖ±½ÓČ”ĮķŅ»ÖÖ²»ÓėĘä·“Ó¦µÄŹŌŅŗ
D. Č”ÓĆ·Ūĩד¹ĢĢå»ņ¹ĢĢ劔æÅĮ£Ź±£¬Ó¦ÓĆŌæ³×»ņÖ½²Ū£¬Č”ÓĆæéד¹ĢĢåŹ±£¬Ó¦ÓĆÄ÷×Ó¼ŠČ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| T/”ę | 20 | 40 | 60 | 80 |
| S£ØLi2CO3£©/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S£ØLi2SO4£©/g | 34.2 | 32.8 | 31.9 | 30.7 |
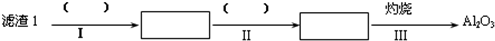
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻõĖįļ§ČÜÓŚĖ® | B£® | ĒāĘųŌŚĀČĘųÖŠČ¼ÉÕ | ||
| C£® | ŃĪĖįŗĶĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦ | D£® | Ba£ØOH£©2•8H2OÓėNH4Cl·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±„ŗĶĢ¼ĖįÄĘČÜŅŗÖŠĶØČė×ćĮæµÄ¶žŃõ»ÆĢ¼£ŗ2Na++CO32-+CO2+H2OØT2NaHCO3”ż | |
| B£® | FeI2ČÜŅŗÖŠµĪČė¹żĮæäåĖ®£ŗ2Fe2++2I-+2Br2ØT2Fe3++I2+4Br- | |
| C£® | NaHSO4ČÜŅŗÖŠµĪČėÉŁĮæBa£ØOH£©2ČÜŅŗ£ŗH++SO42-+Ba2++OH-ØTBaSO4”ż+H2O | |
| D£® | ±„ŗĶŹÆ»ŅĖ®Óė“×ĖįČÜŅŗ»ģŗĻ£ŗCa£ØOH£©2+2CH3COOHØTCa2++2CH3COO-+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | v£ØD£©=0.4 mol/£ØL•min£© | B£® | v£ØB£©=0.6 mol/£ØL•min£© | ||
| C£® | v£ØC£©=0.35 mol/£ØL•min£© | D£® | v£ØA£©=0.5 mol/£ØL•min£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com