
ΓΨΧβΡΩΓΩΘ®1Θ©‘Ύ¥÷÷ΤCuSO4ΓΛ5H2OΨßΧε÷–≥ΘΚ§”–‘”÷ Fe2+ΓΘ‘ΎΧα¥Ω ±ΈΣΝΥ≥ΐ»ΞFe2+Θ§≥ΘΦ”»κΚœ ―θΜ·ΦΝΘ§ ΙFe2+―θΜ·ΈΣFe3+Θ§œ¬Ν–Έο÷ Ω…≤…”ΟΒΡ «________
A. KMnO4 ΓΓ B. H2O2 ΓΓΓΓ C. Cl2 Υ° ΓΓΓΓ D. HNO3
»ΜΚσ‘ΌΦ”»κ Β±Έο÷ Βς’ϊ÷Ν»ή“ΚpH=4Θ§ ΙFe3+ΉΣΜ·ΈΣFe(OH)3Θ§Ω…“‘¥οΒΫ≥ΐ»ΞFe3+Εχ≤ΜΥπ ßCuSO4ΒΡΡΩΒΡΘ§Βς’ϊ»ή“ΚpHΩ…―Γ”Οœ¬Ν–÷–ΒΡ________
A. NaOH B. NH3ΓΛH2O C. CuO D. Cu(OH)2
Θ®2Θ©ΦΉΆ§―ßΜ≥“…Βς’ϊ÷Ν»ή“ΚpH=4 «ΖώΡή¥οΒΫ≥ΐ»ΞFe3+Εχ≤ΜΥπ ßCu2+ΒΡΡΩΒΡΘ§““Ά§―ß»œΈΣΩ…“‘Ά®ΙΐΦΤΥψ»ΖΕ®Θ§Υϊ≤ι‘Ρ”–ΙΊΉ ΝœΒΟΒΫ»γœ¬ ΐΨίΘ§≥ΘΈ¬œ¬Fe(OH)3ΒΡ»ήΕ»ΜΐKsp=8.0ΓΝ10-38,Cu(OH)2ΒΡ»ήΕ»ΜΐKsp=3.0ΓΝ10-20Θ§Ά®≥Θ»œΈΣ≤–Ντ‘Ύ»ή“Κ÷–ΒΡάκΉ”≈®Ε»–Γ”Ύ1ΓΝ10-5 molΓΛL-1 ±ΨΆ»œΈΣ≥ΝΒμΆξ»ΪΘ§…η»ή“Κ÷–CuSO4ΒΡ≈®Ε»ΈΣ3.0 molΓΛL-1Θ§‘ρCu(OH)2ΩΣ Φ≥ΝΒμ ±»ή“ΚΒΡpHΈΣ________Θ§Fe3+Άξ»Ϊ≥ΝΒμ ±»ή“ΚΒΡpHΈΣ________Θ§Ά®ΙΐΦΤΥψ»ΖΕ®…œ ωΖΫΑΗ________Θ®ΧνΓΑΩ…––Γ±ΜρΓΑ≤ΜΩ…––Γ±Θ©(“―÷Σlg2=0.3)
Θ®3Θ©Ά§―ßΟ«”Ο0.1000 molΓΛLΘ≠1ΒΡΥα–‘ΗΏΟΧΥαΦΊ±ξΉΦ»ή“ΚΒΈΕ®Ρ≥ ‘―υ÷–Ιΐ―θΜ·«βΒΡΚ§ΝΩΘ§Ζ¥”Π‘≠άμΈΣ2MnO4Θ≠ΘΪ5H2O2ΘΪ6HΘΪ===2Mn2ΘΪΘΪ8H2OΘΪ5O2ΓϋΓΘ
ΔΌΒΈΕ®ΒΫ¥ο÷’ΒψΒΡœ÷œσ «______________________________________ΓΘ
ΔΎ”Ο“Τ“ΚΙήΈϋ»Γ25.00 mL ‘―υ÷Ο”ΎΉΕ–ΈΤΩ÷–Θ§÷ΊΗ¥ΒΈΕ®ΥΡ¥ΈΘ§ΟΩ¥ΈœϊΚΡΒΡΥα–‘KMnO4±ξΉΦ»ή“ΚΧεΜΐ»γœ¬±μΥυ ΨΘΚ
ΒΎ“Μ¥Έ | ΒΎΕΰ¥Έ | ΒΎ»ΐ¥Έ | ΒΎΥΡ¥Έ | |
ΧεΜΐ(mL) | 17.10 | 18.10 | 17.00 | 16.90 |
‘ρ ‘―υ÷–Ιΐ―θΜ·«βΒΡ≈®Ε»ΈΣ___________molΓΛLΘ≠1ΓΘ
Δέ»τΒΈΕ®«ΑΦβΉλ÷–”–Τχ≈ίΘ§ΒΈΕ®Κσœϊ ßΘ§‘ρ≤βΕ®ΫαΙϊ______(ΧνΓΑΤΪΒΆΓ±ΓΔΓΑΤΪΗΏΓ±ΜρΓΑ≤Μ±δΓ±)ΓΘ
ΓΨ¥πΑΗΓΩ B CD 4 3.3 Ω…–– »ή“Κ”…Έό…Ϊ±δΉœ…ΪΘ§«“ΑκΖ÷÷”ΡΎ≤ΜΜ÷Η¥‘≠…Ϊ 0.1700 ΤΪΗΏ
ΓΨΫβΈωΓΩ ‘ΧβΖ÷ΈωΘΚ±ΨΧβΩΦ≤ι―ΈάύΥ°Ϋβ÷Σ Ε”Π”Ο”ΎΈο÷ ΒΡΖ÷άκΧα¥ΩΘ§»ήΕ»ΜΐΒΡΦΤΥψΘ§―θΜ·ΜΙ‘≠ΒΈΕ® Β―ιΓΘ
Θ®1Θ©AœνΘ§KMnO4ΫΪFe2+―θΜ·ΒΡάκΉ”ΖΫ≥Χ ΫΈΣMnO4-+5Fe2++8H+=Mn2++5Fe3++4H2OΘ§“ΐ»κ‘”÷ άκΉ”Θ§≤Μ≤…”ΟΘΜBœνΘ§H2O2ΫΪFe2+―θΜ·ΒΡάκΉ”ΖΫ≥Χ ΫΈΣ2Fe2++H2O2+2H+=2Fe3++2H2OΘ§≤Μ“ΐ»κ‘”÷ Θ§≤Μ≤ζ…ζΈέ»ΨΈοΘ§Ω…≤…”ΟΘΜCœνΘ§Cl2Υ°ΫΪFe2+―θΜ·ΒΡάκΉ”ΖΫ≥Χ ΫΈΣCl2+2Fe2+=2Cl-+2Fe3+Θ§“ΐ»κ‘”÷ άκΉ”Θ§≤Μ≤…”ΟΘΜDœνΘ§HNO3ΫΪFe2+―θΜ·ΒΡάκΉ”ΖΫ≥Χ ΫΈΣ3Fe2++NO3-+4H+=3Fe3++NOΓϋ+2H2OΘ§≤ζ…ζ¥σΤχΈέ»ΨΈοNOΘ§≤Μ≤…”ΟΘΜΩ…≤…”ΟΒΡ «BΓΘ
NaOHΓΔNH3ΓΛH2OΓΔCuOΓΔCuΘ®OHΘ©2ΕΦΩ…“‘ΒςΫΎ»ή“ΚΒΡpH=4Θ§ΒΪNaOHΓΔNH3ΓΛH2OΜα“ΐ»κ‘”÷ άκΉ”Θ§Υυ“‘―Γ”ΟCuOΜρCuΘ®OHΘ©2Θ§¥πΑΗ―ΓCDΓΘ
Θ®2Θ©CuΘ®OHΘ©2ΩΣ Φ≥ΝΒμ ±άκΉ”ΜΐΒ»”ΎCuΘ®OHΘ©2ΒΡ»ήΕ»ΜΐΘ§Ksp[CuΘ®OHΘ©2]=cΘ®Cu2+Θ©ΓΛc2Θ®OH-Θ©Θ§cΘ®Cu2+Θ©=3mol/LΘ§cΘ®OH-Θ©=![]() =1
=1![]() 10-10mol/LȧcȮH+ȩ=1
10-10mol/LΘ§cΘ®H+Θ©=1![]() 10-4mol/LΘ§CuΘ®OHΘ©2ΩΣ Φ≥ΝΒμ ±»ή“ΚΒΡpH=-lg1
10-4mol/LΘ§CuΘ®OHΘ©2ΩΣ Φ≥ΝΒμ ±»ή“ΚΒΡpH=-lg1![]() 10-4=4ΓΘFe3+Άξ»Ϊ≥ΝΒμ ±cΘ®Fe3+Θ©
10-4=4ΓΘFe3+Άξ»Ϊ≥ΝΒμ ±cΘ®Fe3+Θ©![]() 1
1![]() 10-5mol/LΘ§Ksp[FeΘ®OHΘ©3]=cΘ®Fe3+Θ©ΓΛc3Θ®OH-Θ©Θ§cΘ®OH-Θ©=
10-5mol/LΘ§Ksp[FeΘ®OHΘ©3]=cΘ®Fe3+Θ©ΓΛc3Θ®OH-Θ©Θ§cΘ®OH-Θ©=![]() =2
=2![]() 10-11mol/LȧcȮH+ȩ=5
10-11mol/LΘ§cΘ®H+Θ©=5![]() 10-4mol/LΘ§FeΘ®OHΘ©3Άξ»Ϊ≥ΝΒμ ±»ή“ΚΒΡpH=-lg5
10-4mol/LΘ§FeΘ®OHΘ©3Άξ»Ϊ≥ΝΒμ ±»ή“ΚΒΡpH=-lg5![]() 10-4=3.3ΓΘΗυΨίΦΤΥψΒΡΫαΙϊΘ§…œ ωΖΫΑΗΩ…––ΓΘ
10-4=3.3ΓΘΗυΨίΦΤΥψΒΡΫαΙϊΘ§…œ ωΖΫΑΗΩ…––ΓΘ
Θ®3Θ©ΔΌ”…”ΎKMnO4»ή“Κ±Ψ…μ≥ Ήœ…ΪΘ§ Β―ι÷–≤Μ–η“ΣΦ”÷Η ΨΦΝΘ§ΒΈΕ®ΒΫ¥ο÷’ΒψΒΡœ÷œσ «ΘΚ»ή“Κ”…Έό…Ϊ±δΉœ…ΪΘ§«“ΑκΖ÷÷”ΡΎ≤ΜΜ÷Η¥‘≠…ΪΓΘ
ΔΎ”…”ΎΒΎΕΰ¥Έ Β―ιΈσ≤νΫœ¥σΘ§ΒΎΕΰ¥Έ Β―ι ΐΨί¬‘»ΞΘ§ Β―ι÷–œϊΚΡKMnO4»ή“ΚΧεΜΐΒΡΤΫΨυ÷ΒΈΣ![]() =17.00mLΘ§ Β―ι÷–œϊΚΡnΘ®KMnO4Θ©=0.1mol/L
=17.00mLΘ§ Β―ι÷–œϊΚΡnΘ®KMnO4Θ©=0.1mol/L![]() 0.017L=0.0017molΘ§ΗυΨίΖ¥”Π2MnO4Θ≠ΘΪ5H2O2ΘΪ6HΘΪ=2Mn2ΘΪΘΪ8H2OΘΪ5O2ΓϋΘ§nΘ®H2O2Θ©=
0.017L=0.0017molΘ§ΗυΨίΖ¥”Π2MnO4Θ≠ΘΪ5H2O2ΘΪ6HΘΪ=2Mn2ΘΪΘΪ8H2OΘΪ5O2ΓϋΘ§nΘ®H2O2Θ©=![]() nΘ®KMnO4Θ©=0.00425molΘ§cΘ®H2O2Θ©=0.00425mol
nΘ®KMnO4Θ©=0.00425molΘ§cΘ®H2O2Θ©=0.00425mol![]() 0.025L=0.1700mol/LΓΘ
0.025L=0.1700mol/LΓΘ
Δέ»τΒΈΕ®«ΑΦβΉλ÷–”–Τχ≈ίΘ§ΒΈΕ®Κσœϊ ßΘ§‘ρœϊΚΡΒΡKMnO4»ή“ΚΒΡΧεΜΐΤΪ¥σΘ§≤βΕ®ΫαΙϊΤΪΗΏΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «
A.ΡΤΚΆΦΊΒΡΚœΫπΩ…”Ο”ΎΩλ÷–Ή”Ζ¥”ΠΕ―Ής»»ΫΜΜΜΦΝ
B.Ω…”Ο≥§¥ΩΙη÷Τ‘λΒΡΒΞΨßΙηά¥÷Τ‘λ–ΨΤ§
C.Εΰ―θΜ·ΙηΩ…”Ο”Ύ÷Τ‘λ≤ΘΝß
D.¬»Τχ”–ΕΨΘ§≤ΜΡή”Ο”Ύ“©ΈοΒΡΚœ≥…
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΚλΝΉPΘ®SΘ©ΚΆCl2ΖΔ…ζΖ¥”Π…ζ≥…PCl3ΚΆPCl5Θ§Ζ¥”ΠΙΐ≥ΧΚΆΡήΝΩΙΊœΒ»γΆΦΥυ ΨΘ®ΆΦ÷–ΒΡΓςH±μ Ψ…ζ≥…1mol≤ζΈοΒΡ ΐΨίΘ©ΗυΨί…œΆΦΜΊ¥πœ¬Ν–Έ Χβ

Θ®1Θ©PΚΆCl2Ζ¥”Π…ζ≥…PCl3ΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚ
ΘΜ
Θ®2Θ©PCl5Ζ÷Ϋβ…ζ≥…PCl3ΚΆCl2ΒΡ»»Μ·―ßΖΫ≥Χ ΫΘΚ
ΘΜ
Έ¬Ε»T1 ±Θ§‘ΎΟή±’»ίΤς÷–Φ”»κ0.8mol PCl5 Θ§Ζ¥”Π¥οΒΫΤΫΚβ ±ΜΙ Θ”ύ0.6mol PCl5 Θ§ΤδΖ÷Ϋβ¬ ΠΝ1Β»”Ύ
Θ®3Θ©PΚΆCl2Ζ÷ΝΫ≤ΫΖ¥”Π…ζ≥…1mol PCl5ΒΡΓςH3= ΘΜ
PΚΆCl2“Μ≤ΫΖ¥”Π…ζ≥…1mol PCl5ΒΡΓςH4 ΓςH3(ΧνΓΑ¥σ”ΎΓ±Θ§ΓΑ–Γ”ΎΓ±ΜρΓΑΒ»”ΎΓ±) ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®1Θ©Ά®ΙΐNOx¥ΪΗ–ΤςΩ…Φύ≤βNOxΒΡΚ§ΝΩΘ§ΤδΙΛΉς‘≠άμ Ψ“βΆΦ»γœ¬ΆΦΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΔΌPtΒγΦΪ…œΜΙ–ηΆ®»κΒΡΤχΧε «________ΓΘ
ΔΎ–¥≥ωNiOΒγΦΪΒΡΒγΦΪΖ¥”Π ΫΘΚ_____________________________________________ΓΘ
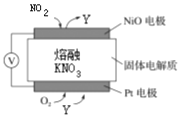
Θ®2Θ©―Έ«≈Βγ≥Ί «“Μ÷÷±»ΫœΤ’±ιΒΡ‘≠Βγ≥ΊΘ§ΗΟΒγ≥ΊΖ¥”Π‘≠άμ»γœ¬ΆΦΥυ ΨΓΘ
ΔΌΗΚΦΪΒγΦΪΖ¥”Π ΫΈΣ________ΓΘ
ΔΎΒ±Βγ¬Ζ÷–Ά®ΙΐΒγΉ”ΈΣ0.1mol ±Θ§ΝΫΒγΦΪ÷ ΝΩ≤νΈΣ___gΘ§¥Υ ±‘≠Βγ≥ΊΒγΫβ÷ »ή“ΚΒΡΉή÷ ΝΩ”κΩΣ Φ ±ΒγΫβ÷ »ή“ΚΉή÷ ΝΩ≤ν÷ΒΈΣ___gΘ®≤ΜΩΦ¬«»ή“ΚάκΉ”œρ―Έ«≈“ΤΕ·Θ©ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ»γΆΦΉΑ÷Ο÷Τ»Γδε±ΫΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
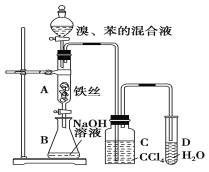
(1)–¥≥ωA÷–Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ_______________________ΘΜ
(2)C÷– ΔΖ≈CCl4ΒΡΉς”Ο «___________________________ΘΜ
(3)D÷–Φ”»κœθΥα“χ»ή“ΚΘ§ Β―ιΚσ»ή“Κ÷–ΡήΩ¥ΒΫΒΡ Β―ιœ÷œσΈΣ_____________________ΘΜ
(4)≥Θ”Ο”ΎΦχ±π±ΫΚΆΦΉ±ΫΒΡ ‘ΦΝΈΣ_________________ΘΜ
(5)EΈο÷ Ζ÷Ή” ΫΈΣC8H10Θ§«“±ΫΜΖ…œΒΡ“Μ¬»¥ζΈο÷Μ”–“Μ÷÷Θ§‘ρEΒΡΟϊ≥ΤΈΣ_____________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΒγάκΖΫ≥Χ Ϋ’ΐ»ΖΒΡ «
A.NaOH=NaΘΪΘΪO2Θ≠ΘΪHΘΪB.FeCl3=Fe3ΘΪΘΪCl3Θ≠
C.Ca(NO3)2=Ca2ΘΪΘΪ2(NO3)2Θ≠D.NH4HSO4=NH4+ΘΪHΘΪΘΪSO42-
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ““ΆιΘ®C2H6Θ©ΉςΈΣ“Μ÷÷–¬Ρή‘¥‘ΎΜ·―ßΝλ”ρ”Π”ΟΙψΖΚΘ§«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ(»γΆΦΥυ ΨΘ§ΉΑ÷ΟΔώΈΣ““Άι»ΦΝœΒγ≥Ί(ΒγΫβ÷ »ή“ΚΈΣKOH»ή“Κ)Θ§Ά®ΙΐΉΑ÷ΟΔρ Βœ÷ΧζΑτ…œΕΤΆ≠ΓΘ
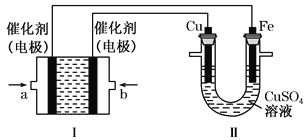
ΔΌa¥Π”ΠΆ®»κ______(ΧνΓΑC2H6Γ±ΜρΓΑO2Γ±)Θ§a¥ΠΒγΦΪ…œΖΔ…ζΒΡΒγΦΪΖ¥”Π Ϋ «____________________________________ΘΜ
ΔΎΒγΕΤΫα χΚσΘ§ΉΑ÷ΟΔώ÷–»ή“ΚΒΡpH______(Χν–¥ΓΑ±δ¥σΓ±ΓΑ±δ–ΓΓ±ΜρΓΑ≤Μ±δΓ±Θ§œ¬Ά§)Θ§ΉΑ÷ΟΔρ÷–Cu2ΘΪΒΡΈο÷ ΒΡΝΩ≈®Ε»______ΘΜ
ΔέΒγΕΤΫα χΚσΘ§ΉΑ÷ΟΔώ»ή“Κ÷–ΒΡ“θάκΉ”≥ΐΝΥOHΘ≠“‘ΆβΜΙΚ§”–___________(Κω¬‘Υ°Ϋβ)ΘΜ‘Ύ¥ΥΙΐ≥Χ÷–»τΆξ»ΪΖ¥”ΠΘ§ΉΑ÷ΟΔρ÷–“θΦΪ÷ ΝΩ±δΜ·12.8 gΘ§‘ρΉΑ÷ΟΔώ÷–άμ¬έ…œœϊΚΡ““Άι________L(±ξΉΦΉ¥Ωωœ¬)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
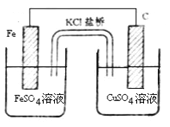
ΓΨΧβΡΩΓΩœ¬Ν–ΗςΉιΈο÷ Α¥ΥαΓΔΦνΓΔ―ΈΖ÷άύΥ≥¥Έ≈≈Ν–Θ°’ΐ»ΖΒΡ «Θ® Θ©
A.ΝρΥαΓΔ¥ΩΦνΓΔΧΦΥαΗΤ
B.œθΥαΓΔ…’ΦνΓΔ ≥―Έ
C.±υ¥ΉΥαΓΔ¥ΩΦνΓΔ¥ΉΥαΡΤ
D.―ΈΥαΓΔ λ ·Μ“ΓΔΩΝ–‘ΡΤ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ’≈«ύΝΪ «Έ“Ιζ÷χΟϊΒΡΜ·―ßΦ“Θ§1991ΡξΥϊΉΦ»Ζ≤βΒΟInΒΡœύΕ‘‘≠Ή”÷ ΝΩΈΣ114.818Θ§±ΜΙζΦ œύΕ‘‘≠Ή”÷ ΝΩΈ·‘±Μα≤…”ΟΈΣ–¬ΒΡ±ξΉΦ÷ΒΓΘœ¬Ν–ΥΒΖ®÷–Θ§¥μΈσΒΡ «Θ® Θ©
A. ![]() In «In‘ΣΥΊΒΡ“Μ÷÷ΚΥΥΊ B.
In «In‘ΣΥΊΒΡ“Μ÷÷ΚΥΥΊ B. ![]() In‘≠Ή”ΚΥΡΎ”–49Ηω÷–Ή”
In‘≠Ή”ΚΥΡΎ”–49Ηω÷–Ή”
C. ![]() In‘≠Ή”ΚΥΡΎ÷ Ή” ΐΚΆ÷–Ή” ΐ÷°ΚΆΈΣ115 D.
In‘≠Ή”ΚΥΡΎ÷ Ή” ΐΚΆ÷–Ή” ΐ÷°ΚΆΈΣ115 D. ![]() In‘≠Ή”ΚΥΆβ”–49ΗωΒγΉ”
In‘≠Ή”ΚΥΆβ”–49ΗωΒγΉ”
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com