
| A. | 在平衡常数表达式中,反应物浓度用起始浓度表示,生成物浓度用平衡浓度表示 | |
| B. | 平衡常数越大,表示化学反应速率越大 | |
| C. | 可以用化学平衡常数来定量描述化学反应的限度 | |
| D. | 平衡常数的大小与温度、浓度、压强、催化剂有关 |
分析 A.在平衡常数表达式中,反应物、生成物都用浓度表示;
B.化学平衡常数大小与化学反应速率大小没有必然关系;
C.化学平衡常数大小决定化学反应进行程度;
D.平衡常数的大小与浓度、压强、催化剂无关.
解答 解:A.在平衡常数表达式中,无论反应物浓度还是生成物浓度都是平衡浓度,故A错误;
B.同一类型的可逆反应化学平衡常数较大,反应物的转化率一定大,但是化学反应速率不一定大,故B错误;
C.化学平衡常数越大,则化学反应限度越大,故C正确;
D.因平衡常数的大小与只与温度有关,与浓度、压强、催化剂无关,故D错误;
故选C.
点评 本题考查了化学平衡及其影响因素,题目难度不大,明确影响化学平衡、化学反应速率的因素为解答关键,注意化学平衡常数与浓度、压强、催化剂无关,为易错点,试题培养了学生的灵活应用基础知识的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 2mL 0.1mol/L的NaOH溶液中滴加2滴0.1mol/L的MgCl2溶液,再滴加2滴0.1mol/L的FeCl3溶液 | 白色沉淀转化为红褐色沉淀 | 溶解度:Mg(OH)2>Fe(OH)3 |
| B | 常温下,相同的铝片分别投入足量的稀、浓硫酸中 | 浓硫酸中铝片先溶解完 | 反应物浓度越大,反应速率越快 |
| C | 向2mL 2%的CuSO4溶液中加入0.5mL 1%的NaOH溶液,振荡后加入几滴有机试剂X的溶液,加热 | 未出现砖红色沉淀 | 有机试剂X中不含醛基 |
| D | NaHCO3溶液与NaAlO2溶液混合 | 生成白色沉淀 | 结合H+的能力:CO32-<AlO2- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入BaCl2溶液,看是否有沉淀生成 | B. | 将水加热煮沸,看是否有沉淀生成 | ||
| C. | 加入NaOH溶液,看是否有沉淀生成 | D. | 加入少量肥皂水,看是否有沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
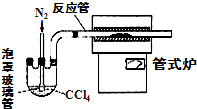 铬主要以铁合金(如铬铁)形式用于生产不锈钢及各种合金钢,铬元素形成的化合物很多,常见的有Cr2O3、CrCl3、H2CrO4,、H2Cr2O7等,请回答下列问题:
铬主要以铁合金(如铬铁)形式用于生产不锈钢及各种合金钢,铬元素形成的化合物很多,常见的有Cr2O3、CrCl3、H2CrO4,、H2Cr2O7等,请回答下列问题: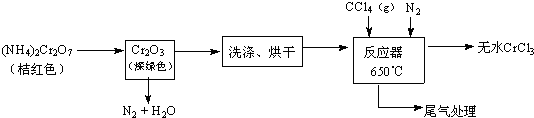
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
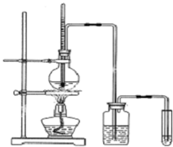 如图是实验室制乙烯并检验其性质的装置图,请回答:
如图是实验室制乙烯并检验其性质的装置图,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
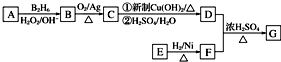
 .
.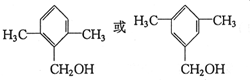 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
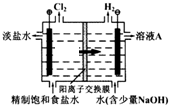 工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水.下图为离子交换膜法电解原理示意图:请回答下列问题:
工业上电解制碱的技术是用离子交换膜法,主要原料是饱和食盐水.下图为离子交换膜法电解原理示意图:请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

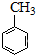 $→_{水溶加热}^{浓H_{2}SO_{4}浓HNO_{3}}$
$→_{水溶加热}^{浓H_{2}SO_{4}浓HNO_{3}}$
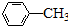 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$
 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$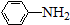 (弱碱性,易被氧化)
(弱碱性,易被氧化) .
.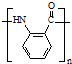 .
. 水解产物的同分异构体,且遇氯化铁溶液发生显色反应,X有3种结构.
水解产物的同分异构体,且遇氯化铁溶液发生显色反应,X有3种结构. →B
→B 等.
等. 的同分异构体:
的同分异构体: 、
、 等
等 属于不同类别
属于不同类别 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com