
��ҵ��һ���ں����ܱ������п��Բ������з�Ӧ�ϳɼ״���
CO(g) �� 2H2(g) ![]() CH3OH(g) �� H
CH3OH(g) �� H
��1���жϷ�Ӧ�ﵽƽ��״̬�������� ������ţ���
a�� ����CH3OH������������CO���������
b�� ���������ܶȲ��� c�� �����������ƽ��������������
d�� CH3OH��CO��H2��Ũ�ȶ����ٷ����仯
��2���±����������Ƿ�Ӧ�ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ����K����
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
���ɱ��������жϦ�H 0 �����������������������
��Ҫ���CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ��_________������ţ���
a������ b��������� c������CO��Ũ��
d������H2��ѹ e��������������ѹ f��������״�
��ij�¶��£���2 mol CO��6 mol H2����2 L���ܱ������У���ַ�Ӧ10min�ﵽƽ��ʱ���c(CO)�� 0.2 mol��L����CO��ת����Ϊ ����ʱ���¶�Ϊ ����CH3OH��ʾ�ù��̵ķ�Ӧ����
v(CH3OH)= mol /��L �� min����
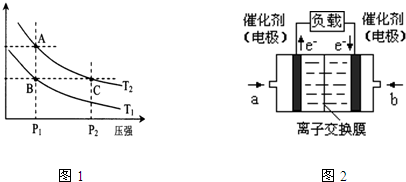
��3��ͼһ��ʾ���¶ȷֱ�ΪT1��T2ʱ��ƽ����ϵ��H2�����������ѹǿ�仯���ߣ�A��C����ķ�Ӧ����A____C�����������������������ͬ����A��C����Ļ�ѧƽ�ⳣ��A_____C����״̬B��״̬A���ɲ���______�ķ���������¡����¡�����


��4��һ�������£�0.5mol�״�������ȫȼ�����ɶ�����̼�����Һ̬ˮ���ų�QKJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ ��
ͼ���Ǽ״�ȼ�ϵ�أ��������ҺΪKOH��Һ���ṹʾ��ͼ��д�� a���缫�Ϸ����ĵ缫��Ӧʽ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 CH3OH��g����H
CH3OH��g����H| �¶� | 250��C | 300��C | 350��C |
| K | 2.041 | 0.270 | 0.012 |
| V2 |
| a2 |
| V2 |
| a2 |
| ���� | �� | �� | �� | |
| ��Ӧ��Ͷ���� | 1molCO��2moL H2 | 1molCH3OH | 2molCH3OH | |
| ƽ �� ʱ �� �� �� |
CH3OHŨ�ȣ�mol/L�� | c1 | c2 | c3 |
| ��Ӧ�������仯 | akJ | bkJ | ckJ | |
| ��ϵѹǿ��Pa�� | p1 | p2 | p3 | |
| ��Ӧ��ת���� | ��1 | ��2 | ��3 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
| ���� |
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
| ���� | �� | �� | �� | |
| ��Ӧ��Ͷ���� | 1molCO��2molH2 | 1molCH3OH | 2molCH3OH | |
| ƽ��ʱ���� | CH3OH��Ũ�ȣ�mol/L�� | c1 | c2 | c3 |
| ��Ӧ�������仯 | akJ | bkJ | ckJ | |
| ��ϵѹǿ��Pa�� | p1 | p2 | p3 | |
| ��Ӧ��ת���� | ��1 | ��2 | ��3 | |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com