



分析 Ⅰ、废铁屑中含有酯类油污,Na2CO3为强碱弱酸盐,CO32-水解生成HCO3-和OH-,升高促进CO32-水解,碱促进油脂水解,然后过滤洗涤,加入稀硫酸,发生反应II为Fe+H2SO4=FeSO4+H2↑,趁热过滤、冷却结晶,过滤洗涤得到FeSO4•7H2O;
Ⅱ、将补血剂研细,向药片中加入稀硫酸,然后过滤得到沉淀,向滤液中加入双氧水,发生反应2Fe2++H2O2+2H+=2Fe3++2H2O,向溶液中加入过量X溶液生成红褐色沉淀,则X为碱,将红褐色沉淀灼烧得到红棕色固体Fe2O3,据此分析解答;
Ⅲ、绿矾中亚铁离子据有还原性;④是尾气处理装置,二氧化硫与NaOH溶液反应;据反应现象可知,绿矾分解生成了二氧化硫、三氧化硫,氧化还原反应中化合价有降必有升,所以有氧化铁生成.
解答 解:Ⅰ、废铁屑中含有酯类油污,Na2CO3为强碱弱酸盐,CO32-水解生成HCO3-和OH-,升高促进CO32-水解,碱促进油脂水解,然后过滤洗涤,加入稀硫酸,发生反应II为Fe+H2SO4=FeSO4+H2↑,趁热过滤、冷却结晶,过滤洗涤得到FeSO4•7H2O;
(1)Na2CO3为强碱弱酸盐,CO32-水解生成HCO3-和OH-,水解方程式为CO32-+H2O?HCO3-+OH-,碳酸根水解呈碱性,在碱性条件下油脂会水解生成易溶于水的物质而被除去,
故答案为:碳酸根水解呈碱性,在碱性条件下油脂会水解生成易溶于水的物质而被除去;
(2)废铁屑中含氧化铁,无需在制备前除去,因为氧化铁和酸反应生成铁盐,铁盐能被Fe还原生成亚铁盐,涉及的离子方程式为Fe2O3+6H+═2Fe3++3H2O、2Fe3++Fe═3Fe2+,故答案为:氧化铁和酸反应生成铁盐,Fe2O3+6H+═2Fe3++3H2O,铁盐能被Fe还原生成亚铁盐2Fe3++Fe═3Fe2+;
Ⅱ、将补血剂研细,向药片中加入稀硫酸,然后过滤得到沉淀,向滤液中加入双氧水,发生反应2Fe2++H2O2+2H+=2Fe3++2H2O,向溶液中加入过量X溶液生成红褐色沉淀,则X为碱,将红褐色沉淀灼烧得到红棕色固体Fe2O3,
(1)配制一定物质的量浓度的溶液时还需要100mL容量瓶,故答案为:100mL容量瓶;
(2)步骤Ⅴ一系列操作依次是:①过滤②洗涤③灼烧④冷却⑤称量⑥恒重操作,操作⑥的目的是确保氢氧化铁完全分解成了氧化铁,
故答案为:灼烧(加热);确保氢氧化铁完全分解成了氧化铁;
(3)ag中m(Fe)=$\frac{112}{160}$×ag=0.7ag,则每片药品中Fe的质量为0.07ag,故答案为:0.07a;
Ⅲ、(1)绿矾中亚铁离子据有还原性,所以最有可能被氧化的元素是Fe;④是尾气处理装置,二氧化硫与NaOH溶液反应,反应的离子方程式为2OH-+SO2=SO32-+H2O 或OH-+SO2=HSO3-,故答案为:Fe;2OH-+SO2=SO32-+H2O 或OH-+SO2=HSO3-;
(2)据反应现象可知,绿矾分解生成了二氧化硫、三氧化硫,氧化还原反应中化合价有降必有升,所以有氧化铁生成,故答案为:b.
点评 本题考查物质的分离和提纯、物质含量的测定,侧重考查分析、计算、基本操作能力,明确每一步发生的反应是解本题关键,知道物质分离和提纯的基本方法,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 序号 | 滴定前读数 | 滴定后读数 |
| 1 | 0.00 | 20.01 |
| 2 | 1.00 | 20.99 |
| 3 | 0.00 | 21.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气中混有二氧化硫(氢氧化钠溶液) | |
| B. | 硫酸亚铁溶液中含有硫酸铜(锌粉) | |
| C. | 二氧化硅中混有石灰石粉末(盐酸) | |
| D. | 二氧化碳中混有二氧化硫(小苏打溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液;X、Y都是惰性电极,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液;X、Y都是惰性电极,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度 | ||
| 浓度(mol/L) | 体积(mL) | 浓度(mol/L) | 体积 (mL) | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
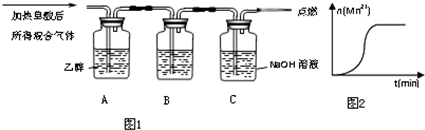
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把氯气通入FeCl2溶液中 | |
| B. | 把绿豆大的钾投入水中 | |
| C. | 把溴水滴加到KI淀粉溶液中 | |
| D. | 把一段打磨过的镁带放入少量冷水中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com