
| A.SO2通入石蕊试液中,溶液由紫色变为无色 |
| B.往氨水中加入NH4Cl固体,溶液pH变小 |
| C.丁达尔效应是胶体的本质特征 |
| D.Al2(SO4)3可除去碱性废水及酸性废水中的悬浮颗粒 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2和CO2都是酸性氧化物,SO2与Na2O2反应生成Na2SO3和O2 |
| B.84 g NaHCO3受热分解,将生成的气体通过足量的Na2O2,固体质量增加31 g |
| C.将Na2O2投入到酚酞试液中,溶液变红 |
| D.Na2O2与水的反应中,Na2O2既是氧化剂,又是还原剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.除①外 | B.除②外 | C.除③外 | D.除⑥外 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用氨气做喷泉实验主要是利用氨气的水溶液呈碱性这一性质 |
| B.某溶液中加入氯化钡溶液和稀硝酸,生成白色沉淀,说明溶液中一定含有SO42- |
| C.浓HNO3与浓H2SO4在空气中长期露置,溶液质量均减轻 |
| D.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.熔融烧碱时不能使用石英坩埚:SiO2 + 2NaOH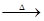 Na2SiO3 + H2O Na2SiO3 + H2O |
| B.在海带灰的浸出液(含有I-)中滴加H2O2得到I2: 2I- +3H2O2 + 2H+ → I2 + O2↑+ 4H2O |
| C.红热的铁丝与水接触,表面形成蓝黑色(或黑色)保护层: 3Fe + 4H2O(g) 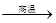 Fe3O4 + 4H2 Fe3O4 + 4H2 |
| D.“84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用时会放出氯气: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com