
运用有关概念判断下列叙述正确的是( )
A.1molH2燃烧放出的热量为H2的燃烧热
B.Na2SO3和H2O2的反应为氧化还原反应
C.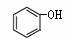 和
和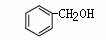 互为同系物
互为同系物
D.BaSO4的水溶液不导电,故BaSO4是弱电解质
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
①11H、21H、31H为三种不同的核素 ②11H、21H、31H互为同位素
③11H、21H、31H互为同素异形体 ④11H、21H、31H同系物
⑤11H、21H、31H同分异构体
⑥同位素的“同位”指核素的质子数相同,在元素周期表中占相同的位置
⑦互为同位素的原子性质相同
A.①②⑥ B.②③⑥ C.①②⑥⑦ D.①②③⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
A.2H2(g)+O2(g)=2H2O(g) △H1;2H2(g)+O2(g)=2H2O(l)△H2
B.S(g)+O2(g)=SO2 (g)△H1;S(s)+O2(g)=SO2(g)△H2
C.C(s)+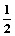 O2(g)=CO (g)△H1;C(s)+O2(g)=CO2(g)△H2
O2(g)=CO (g)△H1;C(s)+O2(g)=CO2(g)△H2
D.H2(g)+Cl2(g)=2HCl(g)△H1;2H2(g)+2Cl2(g)=4HCl(g) △H2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是( )
A.根据某元素原子的质子数和中子数,可以确定该元素的相对原子质量
B.CaCl2、MgCl2晶体都容易潮解,它们潮解的实质是晶体表面吸水形成溶液
C.根据金属活动性顺序表,可以推断冶炼金属时可能的方法
D.根据酸、碱、盐的溶解性表,可以判断某些溶液中的复分解反应能否进行
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化锰可用作干电池去极剂,合成工业的催化剂和氧化剂,玻璃工业和搪瓷工业的着色剂、消色剂、脱铁剂等。
Ⅰ(1)锌—锰碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。电池的总反应式为Zn(s)+2MnO2(s)+H2O(l)===Zn(OH)2(s)+Mn2O3(s)。
电池的正极反应式为________________________________
Ⅱ某化学研究性学习小组拟从废旧干电池中回收二氧化锰制取碳酸锰。
①将干电池剖切、分选得到黑色混合物(主要成分为MnO2)洗涤、过滤、烘干。
②将上述固体按固液体积比2:9加入浓盐酸、加热,反应完全后过滤、浓缩。
③向上述溶液中加入Na2CO3溶液,边加边搅拌,再过滤即可得到碳酸锰。
(2)在第②步中,将上述固体与浓盐酸混合的目的是________________________________
(3)有人认为,将第③步中的Na2CO3溶液换成NH4HCO3溶液,也能达到上述目的,但同时有气体生成。请写出加入NH4HCO3溶液时发生的离子反应方程式:
_______________________________________
Ⅲ 湿法炼锰即电解硫酸锰溶液法。电解锰的生产过程分为化合浸取、氧化净化及沉淀除杂、产品回收。其生产工艺流程如下:
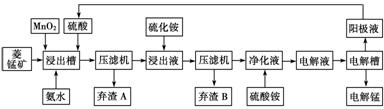
已知:①菱锰矿中主要成份是碳酸锰,主要杂质是Fe2+、Co2+、Ni2+。
②生成氢氧化物的pH如下表:(若某离子浓度小于等于10-5mol/L,则认为完全沉淀)
| 物质 | Fe(OH)2 | Ni(OH)2 | Co(OH)2 | Mn(OH)2 |
| 开始沉淀pH | 7.5 | 7.7 | 7.6 | 8.3 |
| 完全沉淀pH | 9.7 | 8.4 | 8.2 | 9.8 |
③有关难溶氢氧化物和硫化物pKsp数据(pKsp=-lgKsp):
| 难溶物质 | Fe(OH)3 | Ni(OH)2 | Co(OH)2 | NiS | CoS |
| pKsp | 38.55 | 15.26 | 14.7 | 18.49 | 20.40 |
(4)菱锰矿粉与硫酸反应的化学方程式是________________________________。
(5)使用氨水的目的是调节pH值在________之间(填pH范围,精确到小数点后1位数字)。
在“浸出液”中加入(NH4)2S(硫化铵)的目的是_________________________________
(6)电解槽中使用的是惰性电极板,电解反应方程式为_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式与所述事实相符且正确的是( )
A.在强碱性溶液中,次氯酸钠将Mn2+氧化成MnO2:
Mn2++ClO-+H2O===MnO2↓+Cl-+2H+
B.用稀硝酸清洗做过银镜反应的试管:Ag+NO +4H+===Ag++NO↑+2H2O
+4H+===Ag++NO↑+2H2O
C.向FeBr2溶液中通入过量的Cl2:2Fe2++2Br-+2Cl2===2Fe3++Br2+4Cl-
D.用铁棒作阴极、炭棒作阳极电解饱和氯化钠溶液:
2Cl-+2H2O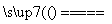 H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验、现象及相关结论均正确的是( )

| 现象 | 品红褪色 | 最后试管有浅黄色沉淀 | 最后一滴溶液使酚酞由无色变为粉红色,且30秒不复原 | 盐桥左端从 无色逐渐变为 蓝色 |
| 结论 |
氧化性 | 有机物中含 有溴原子 | 滴定达到终点 | 金属II比I活泼 |
查看答案和解析>>
科目:高中化学 来源: 题型:
氢气和氟气混合在黑暗处即可发生爆炸而释放出大量的热量。在反应过程中,断裂1molH2中的化学键消耗的能量为Q1kJ,断裂1molF2中的化学键消耗的能量为Q2kJ,形成1molHF中的化学键释放的能量为Q3kJ。下列关系式中正确的是
A.Q1+ Q2<2Q3 B.Q1+ Q2>2Q3 C.Q1+ Q2<Q3 D.Q1+ Q2>Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下:

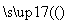

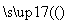

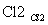
 ―→
―→
(1)实验操作①的名称是 ;实验操作③的名称是________ ,所用主要仪器名称为________。
(2)利用碘的有机溶液得到单质I2的方法是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com