
【题目】氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯商品名称为“特氟龙”,可做不粘锅涂层。它是一种准晶体,该晶体是一种无平移周期序、但有严格准周期位置序的独特晶体。可通过____方法区分晶体、准晶体和非晶体。
(2)基态锑(Sb)原子价电子排布的轨道式为____。[H2F]+[SbF6]—(氟酸锑)是一种超强酸,存在[H2F]+,该离子的空间构型为______,依次写出一种与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是_______、_________。
(3)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序_____(填元素符号)。
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为_____。
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在_______(填序号):
A 离子键 B σ键 C π键 D 氢键 E 范德华力
(4)SF6被广泛用作高压电气设备绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图(见图a)计算相联系的键能。则S—F的键能为_______kJ·mol-1。

(5)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g·cm-3。
①CuF比CuCl熔点高的原因是_____________;
② 已知NA为阿伏加德罗常数。CuF的晶胞结构如上“图b”。则CuF的晶胞参数a=__________nm (列出计算式)。
【答案】X—射线衍射 ![]() V型 H2O NH2- F>N>O>B sp3 AB 327 由两者的熔点可知,CuCl是分子晶体,而CuF为离子晶体,CuF离子晶体的晶格能大于CuCl分子间范德华力
V型 H2O NH2- F>N>O>B sp3 AB 327 由两者的熔点可知,CuCl是分子晶体,而CuF为离子晶体,CuF离子晶体的晶格能大于CuCl分子间范德华力 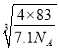 ×107
×107
【解析】
(1)通过X—射线衍射区分晶体、非晶体、准晶体;
(2)根据锑元素原子核外电子排布写出基态锑(Sb)原子价电子排布的轨道式;用价层电子对互斥理论判断[H2F]+的空间构型;用替代法书写与[H2F]+具有相同空间构型和键合形式的分子和阴离子;
(3)①同周期主族元素自左而右原子半径减小,第一电离能呈增大趋势;
②[B(OH)4]﹣中B的价层电子对=4+1/2(3+1-4×1)=4,所以采取sp3杂化;
③NH4BF4(四氟硼酸铵)中含铵根离子和氟硼酸根离子,二者以离子键相结合;铵根离子中含3个σ键和1个配位键,氟硼酸根离子中含3个σ键和1个配位键;
(4)键能指气态基态原子形成1mol化学键释放的最大能量。由图a可知,气态基态S(g)和6F(g)原子形成SF6(g)释放的能量为1962kJ,即形成6molS—F键释放的能量为1962kJ,则形成1molS—F键释放的能量为1962kJ÷6=327kJ,则S—F的键能为327kJ·mol-1;
(5)①CuCl是分子晶体,而CuF为离子晶体,CuF离子晶体的晶格能大于CuCl分子间范德华力,故CuF比CuCl熔点高;
②均摊法计算晶胞中Cu+、F-离子数,计算晶胞质量,晶胞质量=晶体密度×晶胞体积;
(1)从外观无法区分三者,区分晶体、非晶体、准晶体最可靠的方法是X—射线衍射法。本小题答案为:X-射线衍射。
(2)锑为51号元素,Sb位于第五周期VA族,则基态锑(Sb)原子价电子排布的轨道式为![]() ;[H2F]+[SbF6]—(氟酸锑)是一种超强酸,存在[H2F]+,[H2F]+中中心原子F的价层电子对数为2+
;[H2F]+[SbF6]—(氟酸锑)是一种超强酸,存在[H2F]+,[H2F]+中中心原子F的价层电子对数为2+![]() =4,σ键电子对数为2,该离子的空间构型为V型,与[H2F]+具有相同空间构型和键合形式的分子为H2O、阴离子为NH2- 。本小题答案为:
=4,σ键电子对数为2,该离子的空间构型为V型,与[H2F]+具有相同空间构型和键合形式的分子为H2O、阴离子为NH2- 。本小题答案为:![]() ; V型 ;H2O ; NH2-。
; V型 ;H2O ; NH2-。
(3)①H3BO3和NH4BF4涉及的四种元素中第二周期元素是B、N、O、F四种元素,同周期元素从左向右第一电离能呈增大趋势,N的2p能级半充满较稳定,N的第一电离能大于O,则这四种元素第一电离能由大到小的顺序为F>N>O>B。本小题答案为:F>N>O>B。
②[B(OH)4]﹣中B的价层电子对=4+1/2(3+1-4×1)=4,所以B采取sp3杂化。本小题答案为:sp3。
③NH4BF4(四氟硼酸铵)中含铵根离子和氟硼酸根离子,铵根离子中含3个σ键和1个配位键,氟硼酸根离子中含3个σ键和1个配位键,铵根离子和氟硼酸根离子以离子键相结合,则四氟硼酸铵中存在离子键、σ键、配位键。本小题答案为:AB。
(4)键能指气态基态原子形成1mol化学键释放的最大能量。由图a可知,气态基态S(g)和6F(g)原子形成SF6(g)释放的能量为1962kJ,即形成6molS—F键释放的能量为1962kJ,则形成1molS—F键释放的能量为1962kJ÷6=327kJ,则S—F的键能为327kJ·mol-1。本小题答案为:327。
(5)①CuCl的熔点为426℃,熔化时几乎不导电,CuCl是分子晶体,而CuF的熔点为908℃,CuF为离子晶体,CuF离子晶体的晶格能大于CuCl分子间范德华力,故CuF比CuCl熔点高。本小题答案为:由两者的熔点可知,CuCl是分子晶体,而CuF为离子晶体,CuF离子晶体的晶格能大于CuCl分子间范德华力。
②晶胞中Cu+数目为8×1/8+6×1/2=4,F-数目为4,故晶胞质量=(4×64+4×19)g÷NA =(4×83)/NA g,根据![]() =7.1g/cm3×(a ×10-7cm)3,a=
=7.1g/cm3×(a ×10-7cm)3,a=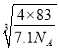 ×107nm。本小题答案为:
×107nm。本小题答案为: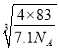 ×107。
×107。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】Na2S2O3·5H2O可作为高效脱氯剂,工业上用硫铁矿(FeS2)为原料制备该物质的流程如图。
![]()
已知:a.气体A可以使品红溶液褪色,与硫化氢(H2S)混合能获得单质硫。
b.pH约为11的条件下,单质硫与亚硫酸盐可以共热生成硫代硫酸盐。
回答下列问题:
(1)吸收塔中的原料B可以选用__(填字母序号)。
A.NaCl溶液 B.Na2CO3溶液 C.Na2SO4溶液
(2)某小组同学用如图装置模拟制备Na2S2O3的过程(加热装置已略去)。

①A中使用70%的硫酸比用98%的浓硫酸反应速率快,其原因是__。装置B的作用是__。
②C中制备Na2S2O3发生的连续反应有:Na2S+H2O+SO2=Na2SO3+H2S,__和Na2SO3+S![]() Na2S2O3。
Na2S2O3。
(3)工程师设计了从硫铁矿获得单质硫的工艺,将粉碎的硫铁矿用过量的稀盐酸浸取,得到单质硫和硫化氢气体,该反应的化学方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年12月,华为宣布: 利用锂离子能在石墨烯表面和电极之间快速大量穿梭运动的特性,开发出石墨烯电池,电池反应式为LixC6+Li1-xCoO2![]() C6+LiCoO2,其工作原理如图所示。下列关于该电池的说法不正确的是
C6+LiCoO2,其工作原理如图所示。下列关于该电池的说法不正确的是

A. 该电池若用隔膜可选用质子交换膜
B. 石墨烯电池的优点是提高电池的储锂容量进而提高能量密度
C. 充电时,LiCoO2极 发生的电极反应为: LiCoO2-xe-=Li1-xCoO2+xLi+
D. 废旧的该电池进行“放电处理”让Li+从石墨烯中脱出而有利于回收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Cl2、NaOH、CO(NH2)2 (尿素)和SO2为原料可制备N2H4·H2O(水合肼)和无水Na2SO3,其主要实验流程如下:

已知:①Cl2+2OH![]() ClO+Cl+H2O是放热反应。
ClO+Cl+H2O是放热反应。
②N2H4·H2O沸点约118 ℃,具有强还原性,能与NaClO剧烈反应生成N2。

(1)如图表示用石墨作电极,在一定条件下电解饱和食盐水制取Cl2时,阳极上产生也会产生少量的ClO2的电极反应式:________________________________;电解一段时间,当阴极产生标准状况下气体112 mL时,停止电解,则通过阳离子交换膜的阳离子物质的量为________mol。
(2)步骤Ⅰ制备NaClO溶液时,若温度超过40℃,Cl2与NaOH溶液反应生成NaClO3和NaCl,其离子方程式为____________________________________;实验中控制温度除用冰水浴外,还需采取的措施是____________________________________。
(3)步骤Ⅱ合成N2H4·H2O的装置如下图所示。NaClO碱性溶液与尿素水溶液在40 ℃以下反应一段时间后,再迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴加的溶液是_________________;使用冷凝管的目的是_________________________________。
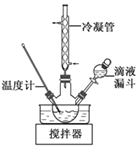
(4)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水Na2SO3,欲测定亚硫酸钠产品的纯度设计如下实验方案,并进行实验。准确称取所得亚硫酸钠样品m g于烧杯中,加入适量蒸馏水配成100 mL待测溶液。移取25.00 mL待测溶液于锥形瓶中,用c mol·L-1酸性KMnO4标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为V mL(假设杂质不反应)。样品中亚硫酸钠的质量分数为__________(用含m、c、V的代数式表示)。某同学设计的下列滴定方式中,合理的是________(夹持部分略去)(填字母序号)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在如图所示的装置中,若通直流电5min时,铜电极质量增加2.16g。试回答下列问题:

(1)电源中X电极为直流电源的________极。
(2)A中发生反应的离子方程式为________。
(3)B中开始电解一段时间后,溶液的pH如何变化_______(填:变大、变小或不变),若要使溶液恢复原状,可向溶液中加入适量的__________。
(4)写出以下电极反应式
①C中的Ag电极___________________.
②B中的阳极______________________.
(5)通电5min时,B中共收集224mL(标准状况下)气体,溶液体积为200mL,则通电前CuSO4溶液的物质的量浓度为(设电解前后溶液体积无变化)__________。
(6)若电解中的直流电源为甲烷燃料电池(KOH为电解质),则电池的负极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血液里Ca2+的浓度一般采用mg·cm-3来表示。抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
(配制KMnO4标准溶液)如图是配制50mL KMnO4标准溶液的过程示意图。


(1)请你观察图示判断,其中不正确的操作有__________(填序号)。
(2)如果用图示的操作配制溶液,所配制的溶液浓度将__________(填“偏大”或“偏小”)。
(测定血液样品中Ca2+的浓度)抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol·L-1 KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液。
(3)已知草酸跟KMnO4溶液反应的离子方程式为2MnO4-+5H2C2O4+6H+=2Mnx++10CO2↑+8H2O则方程式中的x=__________。
(4)经过计算,血液样品中Ca2+的浓度为__________mg·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,下列物质不能与二氧化硅反应的是( )
①焦炭 ②纯碱 ③碳酸钙 ④氢氟酸 ⑤高氯酸 ⑥氢氧化钾 ⑦氧化钙⑧ 氮气
A.③⑤⑦⑧B.⑤⑦⑧C.⑤⑧D.⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C都为短周期元素,它们在周期表中的位置如图所示。已知B、C两元素在周期表中族序数之和是A元素族序数的2倍;B、C元素的原子序数之和是A元素原子序数的4倍,则A、B、C符合的一组是( )

A.铍、钠、铝B.硼、镁、硅C.碳、铝、磷D.氧、磷、氯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可以用高锰酸钾与浓盐酸反应制取氯气,反应方程式如下:
2KMnO4+16HCl = 2KCl+2MnCl2+5Cl2↑+8H2O
请完成下列问题:
(1)在上述方程式中用双线桥法标注电子转移情况____________。
(2)浓盐酸在该反应中表现了____________(选填“氧化性”、“还原性”或“酸性”)。
(3)若15.8g KMnO4与足量的浓盐酸充分反应,则有______mol HCl被氧化,产生的Cl2在标准状况下的体积为__________L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com