
һ������NaHCO3��Na2CO3���������м���500 mL HCl��Һ����Һ�����ԣ����������CO2����4.48 L������������NaHCO3��Na2CO3�������Ⱥ�������(����H2O)�ü�ʯ�����գ���ʯ������4.65 g��������������ȷ����
A������ʱ���ɵ������ڱ����3.36 L
B��NaHCO3��Na2CO3���������Ϊ17.9 g
C������ʱ����Ũ��������������Ũ��������3.3 g
D��HCl��Һ��Ũ��Ϊ0.6 mol��L��1
 ���������������Բ��������ϵ�д�
���������������Բ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1100�棬һ���ݻ����ܱ������з�����Ӧ��FeO(s)+CO(g) Fe(s)+CO2(g)
Fe(s)+CO2(g)
��H=a kJ/mol��a >0�������¶���K=0.263�������йظ÷�Ӧ��˵����ȷ���� ( )
| A��������1 mol Fe�������յ�����С��a kJ B���������¶ȣ�����Ӧ���ʼӿ죬�淴Ӧ���ʼ�������ѧƽ�������ƶ� C����������ѹǿ����ʱ��仯��������жϸ÷�Ӧ�Ѵﵽ��ѧƽ��״̬ D���ﵽ��ѧƽ��״̬ʱ����c(CO)=0.100 mol/L����c(CO2)=0.0263 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������һ����Դ��������Ҫ�ɷ���CH4��0.5 mol CH4��ȫȼ������CO2��Һ̬H2Oʱ���ų�445 kJ���������������Ȼ�ѧ����ʽ��ȷ���ǣ� ��
A.2CH4��g��+4O2(g)====2CO2(g)+4H2O(l) ��H=+890 kJ��mol-1
B.CH4(g)+2O2(g) ====CO2(g)+2H2O(l) ��H=+890 kJ��mol-1
C.CH4(g)+2O2(g) ====CO2��g��+2H2O(l) ��H=-890 kJ��mol-1
D.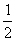 CH4(g)+2O2(g)====
CH4(g)+2O2(g)====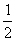 CO2(g)+2H2O(l) ��H=-890 kJ��mol-1
CO2(g)+2H2O(l) ��H=-890 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ȥNaHCO3��Һ�л��е�����Na2CO3�ɲ�ȡ�ķ�����
A��ͨ�������̼���塡�� B����������������Һ
C������  D������ϡ����
D������ϡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��ȷ����
A��Na2CO3��Һ�Լ��ԣ�CO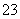 ��2H2O===H2CO3��2OH��
��2H2O===H2CO3��2OH��
B��̼��������Һ�м����������ռ���Һ��HCO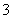 ��OH��===CO
��OH��===CO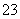 ��H2O
��H2O
C����������ˮ��Ӧ��Na��H2O===Na����OH����H2��
D��H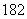 O��Ͷ��Na2O2��2H
O��Ͷ��Na2O2��2H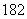 O��2Na2O2===4Na����4OH����18O2��
O��2Na2O2===4Na����4OH����18O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ǻ��õļ����Ԫ�أ��Ƽ��仯�������������������й㷺��Ӧ�á�������м��㣺
(1)��������(NaN3)��ײ����ȫ�ֽ�����ƺ͵������ʿ�Ӧ����������ȫ���ҡ�������40.32 L(��״����)������������Ҫ��������________ g��
(2)�ơ��غϽ���ں˷�Ӧ���������Ƚ���Һ��5.05 g�ơ��غϽ�����200 mLˮ����0.075 mol������
�ټ�����Һ�����������ӵ����ʵ���Ũ��(������Һ����仯)��
�ڼ��㲢ȷ�����ƣ��غϽ�Ļ�ѧʽ��
(3)����������Һ�����������ˣ��õ��������Ƶ���Һ�������Һ��ͨ�������̼�������з�Ӧ��2NaAl(OH)4��CO2�D��2Al(OH)3����Na2CO3��H2O����֪ͨ�������̼336 L(��״����)������24 mol Al(OH)3��15 mol Na2CO3����ͨ����Һ�Ķ�����̼Ϊ112 L(��״ ����)���������ɵ�Al(OH)3��Na2CO3�����ʵ���֮�ȡ�
����)���������ɵ�Al(OH)3��Na2CO3�����ʵ���֮�ȡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������Ȼ���������ͭ�����Һ����ֽ�ϲ�������ʵ�飬ʵ��װ����ͼ��ʾ��
��ش��������⣺
(1)�Թ�������չ��������Ҫ�ɷ���________��
(2)�����������ʵ��Ĺؼ�������������һ����ʱӦע��________��
(3)��������������Ӧ������ɫ��Ӧ����ʵ���ð�ˮ��Ϊ��ɫ�Լ���д����ʵ���н�����ɫ��Ӧ�IJ���������
_____________________________________________��
(4)��ɫ��Ӧ�ɹ۲쵽________��д����ɫ��Ӧʱ��������Ӧ�����ӷ���ʽ��_________________________________________________��
(5)��Ҫ�������ʼ�Ѫ���Ƿ�����Ԫ�أ�ʵ������������£�
��ȡ2 mL���ʼ�Ѫ���������ྻ���������У�����2 mL 2 mol��L��1HNO3��Һ�����Ȳ����Ͻ��衣
�ڽ�������Һ���ɣ��õ������ĩ��
��ȡ���������ĩ����������ϡ�����У����Լ�A���۲������ж�������Ԫ�ش��ڡ�
�����ٵĻ�ѧԭ����________�����о�һ�ֿ����ڲ��������Լ�A������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������̼���ƻ�̼�������ܷ���ˮ�����ʵ�ص���(����)
A��ʵ����ʢ��̼������Һ���Լ�ƿ�����������������ò�����
B����ĭ�������̼��������Һ����������Һ��ʹ��ʱֻ�轫���ϾͿɲ�������������̼����ĭ
C����ϡ������μ��뵽Na2CO3��Һ��,��ʼ������̼�ų�
D������̼�����������ȡ����������̼
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���¼���ʵ�������ȷ���ܴﵽʵ��Ŀ�ĵ���
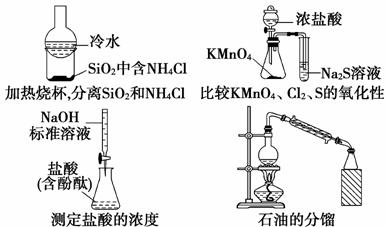
A��1�֡����������������� B��2��
C��3�� D��4��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com