
| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 铝与稀盐酸 | ||
| C. | NaOH与HCl的反应 | D. | 甲烷与O2的燃烧反应 |
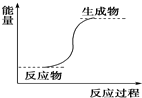
分析 生成物具有的总能量高于反应物具有的总能量,该反应为吸热反应.
①放热反应:有热量放出的化学反应,因为反应物具有的总能量高于生成物具有的总能量.常见放热反应:燃烧与缓慢氧化,中和反应;金属与酸反应制取氢气,生石灰和水反应等.
②吸热反应:有热量吸收的化学反应,因为反应物具有的总能量低于生成物具有的总能量.常见的吸热反应:NH4Cl晶体与Ba(OH)2•8H2O混合搅拌反应,C(s)+H2O(g)→CO(g)+H2O; C+CO2→CO的反应,以及KClO3、KMnO4、CaCO3的分解等.
解答 解:A.NH4Cl晶体与Ba(OH)2•8H2O混合搅拌反应是吸热反应,故A正确;
B.铝与稀盐酸是放热反应,故B错误;
C.酸碱中和反应是放热反应,故C错误;
D.CH4在O2中燃烧反应是放热反应,故D错误;
故选A.
点评 本题考查化学反应的热量变化,学生应注重归纳中学化学中常见的吸热或放热的反应,对于特殊过程中的热量变化的要熟练记忆来解答此类习题,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 一个 | B. | 二个 | C. | 三个 | D. | 四个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温时与锌反应生成大量氢气 | |
| B. | 置于敞口容器中,经过一段时间后质量将减少 | |
| C. | 常温时与铁、铝不反应 | |
| D. | 稀释时将浓硫酸沿器壁慢慢加到水中并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
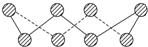 人们研究金星大气成分,发现金星大气中有一种称之为羰基硫(COS)的分子,已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )
人们研究金星大气成分,发现金星大气中有一种称之为羰基硫(COS)的分子,已知羰基硫分子中所有原子的最外层都满足8电子结构,结合已学知识,判断有关说法正确的是( )| A. | 羰基硫属于非极性分子 | |
| B. | 羰基硫的电子式为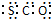 | |
| C. | 羰基硫的沸点比CO2低 | |
| D. | 羰基硫分子中三个原子处于同一直线上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
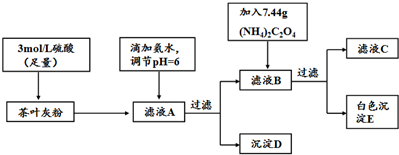
| 离子 | Ca2+ | Fe3+ |
| 完全沉淀时的pH | 13 | 3.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com