
【题目】氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如图:
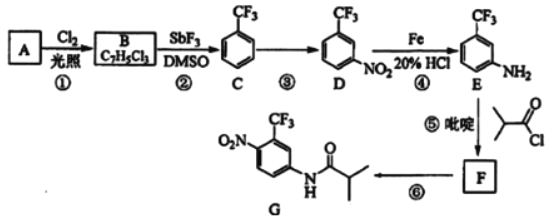
回答下列问题:
(1)A的结构简式为__。C的化学名称是__。
(2)③的反应试剂和反应条件分别是__,该反应的类型是__。
(3)⑤的反应方程式为__。吡啶是一种有机碱,其作用是__。
(4)G的分子式为__。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有__种。
(6)4甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备4甲氧基乙酰苯胺的合成路线__(其他试剂任选)。
)制备4甲氧基乙酰苯胺的合成路线__(其他试剂任选)。
【答案】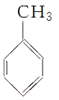 三氟甲苯 浓HNO3/浓H2SO4、加热 取代反应
三氟甲苯 浓HNO3/浓H2SO4、加热 取代反应 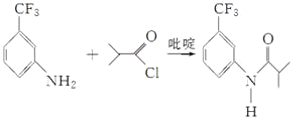 +HCl 吸收反应产生的HCl,提高反应转化率 C11H11O3N2F3 9
+HCl 吸收反应产生的HCl,提高反应转化率 C11H11O3N2F3 9 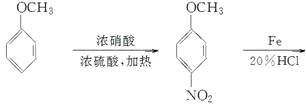

【解析】
A和氯气在光照的条件下发生取代反应生成B,B的分子式为C7H5Cl3,可知A的结构中有3个氢原子被氯原子取代,B与SbF3发生反应生成![]() ,说明发生了取代反应,用F原子取代了Cl原子,由此可知B为
,说明发生了取代反应,用F原子取代了Cl原子,由此可知B为![]() ,进一步可知A为
,进一步可知A为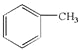 ,
,![]() 发生消化反应生成了
发生消化反应生成了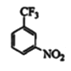 ,
, 被铁粉还原为
被铁粉还原为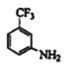 ,
, 与吡啶反应生成F,最终生成
与吡啶反应生成F,最终生成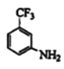 ,由此分析判断。
,由此分析判断。
(1)由反应①的条件、产物B的分子式及C的结构简式,可逆推出A为甲苯,结构为 ;C可看作甲苯中甲基中的三个氢原子全部被氟原子取代,故其化学名称为三氟甲(基)苯;
;C可看作甲苯中甲基中的三个氢原子全部被氟原子取代,故其化学名称为三氟甲(基)苯;
(2)对比C与D的结构,可知反应③为苯环上的硝化反应,因此反应试剂和反应条件分别是浓HNO3/浓H2SO4、加热,反应类型为取代反应;
(3)对比E、G的结构,由G可倒推得到F的结构为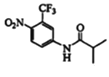 ,然后根据取代反应的基本规律,可得反应方程式为:
,然后根据取代反应的基本规律,可得反应方程式为: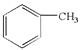 +HCl,吡啶是碱,可以消耗反应产物HCl;
+HCl,吡啶是碱,可以消耗反应产物HCl;
(4)根据G的结构式可知其分子式为C11H11O3N2F3;
(5)当苯环上有三个不同的取代基时,先考虑两个取代基的异构,有邻、间、对三种异构体,然后分别在这三种异构体上找第三个取代基的位置,共有10种同分异构体,除去G本身还有9种。
(6)对比原料和产品的结构可知,首先要在苯环上引入硝基(类似流程③),然后将硝基还原为氨基(类似流程④),最后与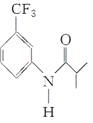 反应得到4甲氧基乙酰苯胺(类似流程⑤),由此可得合成路线为:
反应得到4甲氧基乙酰苯胺(类似流程⑤),由此可得合成路线为: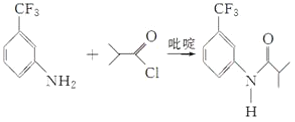
 。
。


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:
【题目】下列解释工业生产或应用的化学方程式正确的是( )
A.氯碱工业制氯气:2NaCl(熔融)![]() 2Na+C12↑
2Na+C12↑
B.利用磁铁矿冶炼铁:CO+FeO![]() Fe+CO2
Fe+CO2
C.工业制小苏打:NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl
D.工业制粗硅:C+SiO2![]() Si+CO2↑
Si+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列关于NaOH溶液和氨水的说法正确的是( )
A.25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为20:1
B.pH=13的两溶液稀释100倍,pH都为11
C.两溶液中分别加入少量NH4Cl固体,c(OH )均减小
D.体积相同、pH相同的两溶液能中和等物质的量的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是( )
A.除去Cl2中含有的少量HCl 
B.蒸干FeCl3饱和溶液制备FeCl3晶体
C.制取少量纯净的CO2气体
D.分离CCl4萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化镓(GaN)被称为第三代半导体材料,其应用已经取得了突破性的进展。
已知:(i)氮化镓性质稳定,不与水、酸反应,只在加热时溶于浓碱。
(ii)NiCl2 溶液在加热时,先转化为Ni(OH)2,后分解为NiO。
(iii)制备氮化镓的反应为:2Ga+2NH3![]() 2GaN+3H2
2GaN+3H2
某学校化学兴趣小组实验室制备氮化镓,设计实验装置如图所示:
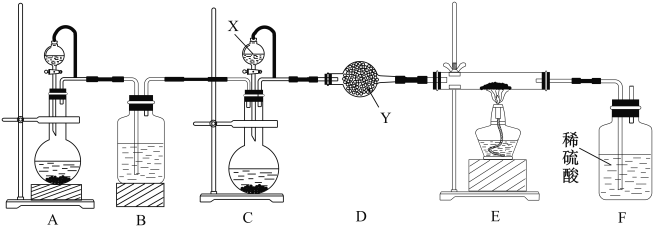
设计实验步骤如下:
①滴加几滴NiCl2 溶液润湿金属镓粉末,置于反应器内。
②先通入一段时间后的H2,再加热。
③停止通氢气,改通入氨气,继续加热一段时间。
④停止加热,继续通入氨气,直至冷却。
⑤将反应器内的固体转移到盛有盐酸的烧杯中,充分反应过滤、洗涤、干燥。
(1)仪器X中的试剂是___________,仪器Y的名称是__________________。
(2)指出该套装置中存在一处明显的错误是________________________。
(3)步骤①中选择NiCl2 溶液,不选择氧化镍的原因是____________________。
a.增大接触面积,加快化学反应速率
b使镍能均匀附着在镓粉的表面,提高催化效率
c.为了能更好形成原电池,加快反应速率
(4)步骤③中制备氮化镓,则判断该反应接近完成时观察到的现象是____________________。
(5)请写出步骤⑤中检验产品氮化镓固体洗涤干净的操作________________________。
(6)镓元素与铝同族,其性质与铝类似,请写出氮化镓溶于热NaOH溶液的离子方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅及其化合物用广泛,请回答下列相关问题:
(1)铅是碳的同族元素,比碳多4个电子层。铅元素的原子结构示意图为____________;相同温度下,同浓度的![]() 溶液和
溶液和![]() 溶液中水的电离程度___________(填“前者大”“后者大”或“一样大”)。
溶液中水的电离程度___________(填“前者大”“后者大”或“一样大”)。
(2)工业上利用锌冶炼过程中的铅浮渣(主要成分是![]() 、
、![]() ,含有少量
,含有少量![]() 、
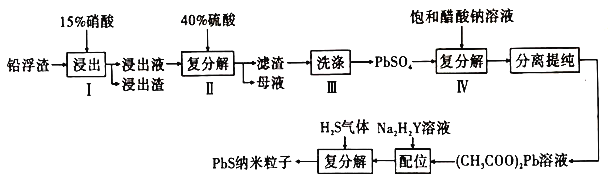
、![]() 和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示:
和其他不溶于硝酸的杂质)生产硫酸铅和硫化铅纳米粒子,流程如图所示:
已知:a.25℃时,![]() ,
,![]() ,
,![]() 。
。
b.![]() 二钠简写成
二钠简写成![]() ,可以与
,可以与![]() 及其他许多金属离子形成稳定的配离子。
及其他许多金属离子形成稳定的配离子。
①已知步骤Ⅰ有![]() 产生,
产生,![]() 被足量稀硝酸氧化成
被足量稀硝酸氧化成![]() 。写出
。写出![]() 参加反应的离子方程式:________。
参加反应的离子方程式:________。
②步骤Ⅰ需控制硝酸的用量并使![]() 稍有剩余,原因是_________________________。
稍有剩余,原因是_________________________。
③硫酸铅微溶于水,醋酸铅易溶于水,步骤Ⅳ能发生反应的原因是____________________。
④不用硫化氢气体直接通入![]() 溶液来制备
溶液来制备![]() 纳米粒子的原因是__________________。
纳米粒子的原因是__________________。
⑤已知铅蓄电池工作时会产生![]() ,则铅蓄电池
,则铅蓄电池![]() 充电时的阳极反应式为________________________________。
充电时的阳极反应式为________________________________。
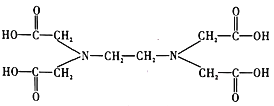
⑥![]() 又名乙二氨四乙酸,是一种弱酸(结构如图),在水溶液中可形成内盐(总电荷为0,电中性的化合物,但是带正电和负电的原子不同)。据此写出
又名乙二氨四乙酸,是一种弱酸(结构如图),在水溶液中可形成内盐(总电荷为0,电中性的化合物,但是带正电和负电的原子不同)。据此写出![]() 的结构:_________________。
的结构:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚石、石墨烯和![]() 都是碳的同素异形体,其结构示意图如图:
都是碳的同素异形体,其结构示意图如图:

(1)金刚石属立方晶系,每个晶胞所包括的C原子个数为_____________。
(2)金刚石、石墨烯、木炭和![]() 都是由碳元素组成的单质。下列关于碳的单质的叙述正确的是_______(填序号)。
都是由碳元素组成的单质。下列关于碳的单质的叙述正确的是_______(填序号)。
A.都是黑色固体
B.碳原子的排列方式不相同
C.这四种物质都很软,可作润滑剂
D.在氧气中充分燃烧时都生成二氧化碳
E.一定条件下,木炭转化成金刚石是物理变化
(3)金刚石质硬但脆,金刚石能被砸碎的原因是_______________________________。
(4)观察计算一个![]() 分子结构中含有____________个正五边形和_________个正六边形。
分子结构中含有____________个正五边形和_________个正六边形。
(5)石墨烯是单层的石墨,它是世界上已知的最薄、最坚硬的新型材料,有良好的导电性,具有很好的应用前景。石墨烯中碳原子的杂化轨道类型为___________;碳碳键的键角是___________。
(6)碳化硅(![]() )的结构与金刚石类似,设碳化硅的密度为
)的结构与金刚石类似,设碳化硅的密度为![]() ,碳化硅晶体内碳硅键的键长为________________
,碳化硅晶体内碳硅键的键长为________________![]() (用NA表示阿伏加德罗常数的值,列表达式即可)。
(用NA表示阿伏加德罗常数的值,列表达式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定体积的密闭容器中,加入2mol A和1mol B发生可逆反应2A(g)+B(g)3C(g)+D(g),达到平衡,C的浓度为w mol/L。若维持容器体积和温度不变,下列四种配比作为起始物质,达平衡后,C的浓度仍为w mol/L的是( )
A.4 mol A+2 mol B B.1 mol B+3 mol C+1 mol D
C.3 mol C+2 mol D D.1 mol A+0.5 mol B+1.5 mol C+0.5 mol D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol·L-1的AgNO3溶液分别滴定体积均为50.0mL的由Cl-与Br-组成的混合溶液和由C1-与I-组成的混合溶液(两混合溶液中Cl-浓度相同,Br-与I-的浓度也相同),其滴定曲线如图所示。已知25℃时:Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=4.9×10-13,Ksp(AgI)=8.5×10-16。
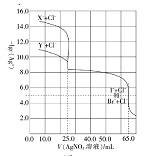
下列有关描述正确的是( )
A.图中X-为Br-
B.混合溶液中n(Cl-):n(I-)=8:5
C.滴定过程中首先沉淀的是AgCl
D.当滴入AgNO3溶液25mL时,Cl-与Br-组成的混合溶液中c(Ag+)=7×10-7mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com