
|
已知反应的化学方程式aFeCl2+bKNO3+cHCl | |
| [ ] | |
A. |
N2 |
B. |
NH4Cl |
C. |
NO |
D. |
NO2 |
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
 氮氧化物是大气污染物之一,消除氮氧化物的方法有多种.
氮氧化物是大气污染物之一,消除氮氧化物的方法有多种.| 180℃ |
| 催化剂 |
| ClO2 |
| 反应Ⅰ |
| Na2SO3 |
| 反应Ⅱ |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年福建省漳州市八校高三第三次联考理综化学试卷(解析版) 题型:填空题
氮氧化物是大气污染物之一,消除氮氧化物的方法有多种。
(1)利用甲烷催化还原氮氧化物。已知:
①CH4 (g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)?? △H =-574 kJ/mol
②CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g)? △H =-1160 kJ/mol
则CH4 将NO2 还原为N2 的热化学方程式为:??????????? ???????????? 。
 (2)利用NH3催化还原氮氧化物(SCR技术)。该技术是目前应用最广泛的烟气氮氧化物脱除技术。 反应的化学方程式为:
(2)利用NH3催化还原氮氧化物(SCR技术)。该技术是目前应用最广泛的烟气氮氧化物脱除技术。 反应的化学方程式为: 为提高氮氧化物的转化率可采取的措施是???????? ????????????????????????? (写出1条即可)。
为提高氮氧化物的转化率可采取的措施是???????? ????????????????????????? (写出1条即可)。
(3)利用ClO2 氧化氮氧化物。其转化流程如下:? NO NO2
NO2 N2。已知反应Ⅰ的化学方程式为2NO+ ClO2 + H2O =NO2 + HNO3 + HCl,则反应Ⅱ的化学方程式是???????? ????? ;若生成11.2 L N2(标准状况),则消耗ClO2 ??????? g 。
N2。已知反应Ⅰ的化学方程式为2NO+ ClO2 + H2O =NO2 + HNO3 + HCl,则反应Ⅱ的化学方程式是???????? ????? ;若生成11.2 L N2(标准状况),则消耗ClO2 ??????? g 。
(4)用活性炭还原法处理氮氧化物.有关反应为:C(s)+2NO(g) N2 (g)+CO2 (g)△H.某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2 (g)+CO2 (g)△H.某研究小组向某密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol?L-1/ 时间/min | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
50 | 0.032 | 0.034 | 0.017 |
①T1℃时,该反应的平衡常数K= ????????? (保留两位小数).②30min后,改变某一条件,反应重新达到平衡,则改变的条件可能是 ????????????? .③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则该反应的△H ?? 0(填“>”、“=”或“<”).
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖南省怀化市高三第一次模拟考试理综化学试卷(解析版) 题型:填空题
氮氧化物是大气污染物之一,消除氮氧化物的方法有多种。
(1)利用甲烷催化还原氮氧化物。已知:
CH4 (g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)??? △H =-574 kJ/mol
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g)?? △H =-1160 kJ/mol
则CH4 将NO2 还原为N2 的热化学方程式为??????????????????????????????? 。???????
 (2)利用NH3催化还原氮氧化物(SCR技术)。该技术是目前应用最广泛的烟气氮氧化物脱除技术。 反应的化学方程式为:2NH3(g)+NO(g)+NO2(g)
(2)利用NH3催化还原氮氧化物(SCR技术)。该技术是目前应用最广泛的烟气氮氧化物脱除技术。 反应的化学方程式为:2NH3(g)+NO(g)+NO2(g)  ? 2N2(g)+3H2O(g) ΔH < 0
? 2N2(g)+3H2O(g) ΔH < 0
为提高氮氧化物的转化率可采取的措施是????????????????? (写出1条即可)。
(3)利用ClO2 氧化氮氧化物。其转化流程如下:
NO NO2
NO2 N2
N2
已知反应Ⅰ的化学方程式为2NO+ ClO2 + H2O = NO2 + HNO3 + HCl,则反应Ⅱ的化学方程式是?? ????????????? ;若生成11.2 L N2(标准状况),则消耗ClO2 ??????? g 。
(4)利用CO催化还原氮氧化物也可以达到消除污染的目的。
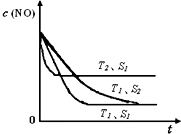
已知质量一定时,增大固体催化剂的表面积可提高化学反应速率。如图是反应2NO(g) + 2CO(g)  2CO2(g)+ N2(g) 中NO的浓度随温度(T)、等质量催化剂表面积(S)和时间(t)的变化曲线。据此判断该反应的△H????? 0 (填“>”、“<”或“无法确定”);催化剂表面积S1????? S2 (填“>”、“<”或“无法确定”)。
2CO2(g)+ N2(g) 中NO的浓度随温度(T)、等质量催化剂表面积(S)和时间(t)的变化曲线。据此判断该反应的△H????? 0 (填“>”、“<”或“无法确定”);催化剂表面积S1????? S2 (填“>”、“<”或“无法确定”)。

查看答案和解析>>
科目:高中化学 来源: 题型:
以富含硫酸亚铁的工业废液为原料生产氧化铁的工艺如下(部分操作和条件略):
Ⅰ.从废液中提纯并结晶出![]() 。
。
Ⅱ.将![]() 配制成溶液。www..com
配制成溶液。www..com
Ⅲ.![]() 溶液与稍过量的
溶液与稍过量的![]() 溶液混合,得到含
溶液混合,得到含![]() 的浊液,同时有CO2气体
的浊液,同时有CO2气体
放出。
Ⅳ.将浊液过滤,用90℃热水洗涤沉淀,干燥后得到![]() 固体。
固体。
Ⅴ.煅烧![]() ,得到
,得到![]() 固体。
固体。
已知:![]() 在热水中分解。
在热水中分解。
(1)Ⅰ中,加足量的铁屑除去废液中的![]() ,该反应的离子方程式是 。
,该反应的离子方程式是 。
(2)Ⅱ中,需加一定量硫酸。运用化学平衡原理简述硫酸的作用 。
(3)Ⅲ中,生成![]() 的离子方程式是 。若
的离子方程式是 。若![]() 浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是 。
浊液长时间暴露在空气中,会有部分固体表面变为红褐色,该变化的化学方程式是 。
(4)Ⅳ中,通过检验![]() 来判断沉淀是否洗涤干净。检验
来判断沉淀是否洗涤干净。检验![]() 的操作是 。
的操作是 。
(5)已知锻炼![]() 的化学方程式是
的化学方程式是![]()
![]()
![]() 。现锻炼464.0kg
。现锻炼464.0kg
的![]() ,得到316.8kg产品。若产品中杂质只有
,得到316.8kg产品。若产品中杂质只有![]() ,则该产品中
,则该产品中![]() 的质量是
的质量是
kg。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com