
【题目】丁二酮肟 ![]() 是检验Ni2+的灵敏试剂.
是检验Ni2+的灵敏试剂.
(1)Ni2+基态核外电子排布式为 . 丁二酮肟分子中C原子轨道杂类型为 , 1mol丁二酮肟分子所含σ键的数目为 .
(2)Ni能与CO形成四羰基镍[Ni(CO)4],四羰基镍熔点﹣19.3℃,沸点42.1℃,易溶于有机溶剂.
①Ni(CO)4固态时属于晶体(填晶体类型).
②与CO互为等电子体的阴离子为(填化学式).
(3)Ni2+与Mg2+、O2﹣形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为 . 
【答案】
(1)1s22s22p63s23p63d8;sp3和sp2;15NA
(2)分子;CN﹣
(3)Mg2NiO3
【解析】解:(1)Ni是28号元素,根据原子核外电子排布规律可知,Ni2+的基态核外电子排布式为1s22s22p63s23p63d8 , 甲基上碳原子价层电子对个数是4且不含孤电子对,为sp3杂化,连接甲基的碳原子含有3个价层电子对且不含孤电子对,为sp2杂化,已知丁二酮肟的结构式为 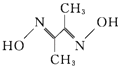 ,分子中含有13个单键,和2个双键,则共含有15个σ键,所以1mol丁二酮肟含有σ键数目为15NA;所以答案是:1s22s22p63s23p63d8;sp3和sp2;15NA;(2)①分子晶体的熔沸点较低,四羰基镍熔点﹣19.3℃,沸点42.1℃,所以该物质为分子晶体,
,分子中含有13个单键,和2个双键,则共含有15个σ键,所以1mol丁二酮肟含有σ键数目为15NA;所以答案是:1s22s22p63s23p63d8;sp3和sp2;15NA;(2)①分子晶体的熔沸点较低,四羰基镍熔点﹣19.3℃,沸点42.1℃,所以该物质为分子晶体,
所以答案是:分子;②由第二周期主族元素组成的且与CO互为等电子体的阴离子为CN﹣ ,
所以答案是:CN﹣;(3)氧离子位于该晶胞的棱上,氧离子个数= ![]() ×12=3,所以该晶胞含有3个氧离子;镁离子处在面上,镁离子个数=
×12=3,所以该晶胞含有3个氧离子;镁离子处在面上,镁离子个数= ![]() ×4=2,该晶胞中含有2个镁离子,根据化学式中元素化合价代数和为零,该晶胞中含有1个Ni,所以该晶胞的化学式为Mg2NiO3 ,
×4=2,该晶胞中含有2个镁离子,根据化学式中元素化合价代数和为零,该晶胞中含有1个Ni,所以该晶胞的化学式为Mg2NiO3 ,
所以答案是:Mg2NiO3 .


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:
【题目】如图,在玻璃管中放入还原铁粉和石棉绒的混合物,加热并通入水蒸气,用试管收集产生的经干燥的水蒸气,并靠近火焰点燃。
(1)写出该反应的化学方程式 , 氧化剂是。
(2)加热烧瓶的作用是 , 烧瓶底部放了几片碎瓷片,其作用是。干燥管里可装入的试剂是 , 其作用是。
(3)实验开始时应先点燃(填“酒精灯”或“酒精喷灯”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知还原性:SO32﹣>I﹣ . 向含有amolKI和amolK2SO3的混合液中通入bmolCl2充分反应(不考虑Cl2与I2之间的反应).下列说法不正确的是( )
A.当a≥b时,发生的离子反应为SO32﹣+Cl2+H2O=SO42﹣+2H++2Cl﹣
B.当5a=4b时,发生的离子反应为SO32﹣+2I﹣+5Cl2+4H2O=4SO42﹣+I2+8H++10Cl﹣
C.当a≤b≤ ![]() a时,反应中转移电子的物质的量n(e﹣)为amol≤n(e﹣)≤3amol
a时,反应中转移电子的物质的量n(e﹣)为amol≤n(e﹣)≤3amol
D.当a<b< ![]() a时,溶液中SO42﹣、I﹣与Cl﹣的物质的量之比为a:(3a﹣2b):2b
a时,溶液中SO42﹣、I﹣与Cl﹣的物质的量之比为a:(3a﹣2b):2b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在10L容器中,加入2mol的SO2(g)和2mol的NO2(g),保持温度恒定,发生反应:SO2(g)+NO2(g)SO3(g)+NO(g).当达到平衡状态时,测得容器中SO2(g)的转化率为50%.
试求:该温度下、该容器中,再继续加入1mol的SO2(g),则:
(1)化学平衡将向方向移动,NO2的转化率将(填“增大”、“不变”或“减小”);
(2)经计算,当达到新的平衡状态时,容器中SO2(g)的浓度是mol/L;
(3)整个过程中,SO2的转化率由50%变为%,NO2的转化率由%变为%.
(4)计算结果给我们的启示是:增大一种反应物物的用量,其转化率将(填“增大”、“不变”或“减小”)另一反应物的转化率将(填“增大”、“不变”或“减小”).现实生产中的意义是:可以通过增大的用量,来提高成本高的反应物的利用率.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活.
已知:
①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l);△H=﹣2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=﹣566kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的△H= .
(2)依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2﹣ . 在电池内部O2﹣移动方向和在电池负极反应的物质分别是
A.正极;O2
B.负极;C3H8
C.正极;C3H8
D.负极;O2
(3)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:CO (g)+H2O(g)CO2(g)+H2 (g)
①下列事实能说明该反应达到平衡的是 .
a.体系中的压强不发生变化 b.υ正(H2)=υ逆(CO)
c.混合气体的平均相对分子质量不发生变化 d.CO2的浓度不再发生变化
②T℃时,在1L的容器中,通入一定量的CO(g)和H2O(g),发生反应并保持温度不变,各物质浓度随时间变化如表:
时间/min | c(CO) | c(H2O)(g) | c(CO2) | c(H2) |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | 0.100 | 0.200 | 0.100 | 0.100 |
4 | 0.100 | 0.200 | 0.100 | 0.100 |
计算2min内用CO表示的该反应速率v=;4min时保持其它条件不变,向上述平衡体系中加入0.1molCO、0.1molCO2、0.1molH2 , 此时反应将向向进行(填“正”或“逆”).
③已知420℃时,该化学反应的平衡常数为9.如果反应开始时CO和H2O(g)的浓度都是0.01mol/L,则CO在此条件下的转化率为 . 又知397℃时该反应的平衡常数为12,请判断该反应的△H0 (填“>”、“=”、“<”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
A.标准状况下,2.24L SO3中含有的SO3分子数为0.1NA
B.5.6 g Fe与标准状况下2.24L的Cl2充分反应,转移的电子数为0.3NA
C.将含3NA个离子的Na2O2固体溶于水配成1L溶液,所得溶液中Na+的浓度为2mol/L
D.1molMnO2与4mol浓盐酸充分反应后生成的Cl2分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)某密闭容器中发生反应:X(g)+Y(g)3Z(g)△H<0如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( ) 
A.t2时加入了催化剂
B.t3时降低了温度
C.t5时增大了压强
D.t4~t5时间内转化率最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关气体摩尔体积的描述中正确的是 ( )
A. 单位物质的量的气体所占的体积就是气体摩尔体积
B. 通常状况下的气体摩尔体积约为22.4L
C. 标准状况下的气体摩尔体积约为22.4L
D. 相同物质的量的气体摩尔体积也相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制0.1molL﹣1NaCl溶液,下列操作会导致所配溶液的物质的量浓度偏高的是( )
A.称量时,左盘低,右盘高
B.定容时俯视读取刻度
C.原容量瓶洗净后未干燥
D.定容时液面超过了刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com