(1)钢铁制品表面“发蓝”技术的化学反应过程中,包括的化学反应有:
①3Fe+NaNO
2+5NaOH=3Na
2FeO
2+H
2O+NH
3②6Na
2FeO
2+NaNO
2+5H
2O=3Na
2Fe
2O
4+NH
3↑+7NaOH
③Na
2FeO
2+Na
2Fe
2O
4+2H
2O=Fe
3O
4+4NaOH.则1mol铁失去
mole
-生成Fe
3O
4(2)在反应15CuSO
4+11P+24H
2O=5Cu
3P+6H
3PO
4+15H
2SO
4中,1molCuSO
4氧化
molP
(3)向一定量由Fe、FeO、Fe
2O
3、Fe
3O
4组成的混合物中加入10mL10mol/LHCl,混合物恰好完全溶解,放出224mL(STP)H
2.反应后的溶液中加入KSCN溶液,无血红色出现.若用足量的CO高温下还原相同质量的此混合物,则还原所得到铁的质量为
g
| Na、Mg、Al的物质的量x | x< | <x<1 | ③ | ④ |
| 产生H2的体积 | ① | ② | V(Na)>V(Mg)=V(Al) | V(Na)=V(Mg)=V(Al) |
(4)等物质的量的金属(M):Na、Mg、Al,分别与1L1mol/LHCl反应,产生相同状况下H
2体积分别为V(Na)、V(Mg)、V(Al).
当n(M)取不同数值时,填写表中①、②处与产生V(H
2)关系;
当已知V(Na)、V(Mg)、V(Al)的关系时,计算③、④处的x取值范围.

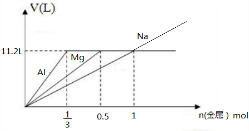 ,结合图象分析计算.
,结合图象分析计算. ,则:
,则:

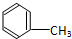 C:CH3CH2OH
C:CH3CH2OH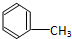 在浓硫酸作用下,与浓硝酸共热至100℃反应的化学方程式为:
在浓硫酸作用下,与浓硝酸共热至100℃反应的化学方程式为: