
分析 (1)放电时,正极上PbO2得电子;
(2)该电池反应中,铜失电子发生氧化反应,作负极;根据电极方程式计算;
(3)原电池中失电子的一极为负极;
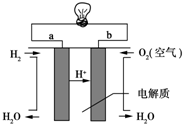
(4)①氢氧燃料电池的正极是氧气得电子发生还原反应;
②根据燃料电池的总反应方程式判断硫酸浓度的变化.
解答 解:(1)放电时,正极上PbO2得电子,正极反应式为PbO2+4H++SO42-+2e-═PbSO4+2H2O,
故答案为:PbO2+4H++SO42-+2e-═PbSO4+2H2O;
(2)该电池反应中,铜失电子发生氧化反应,作负极;负极反应式为Cu-2e-=Cu2+,则当线路中转移0.2mol电子时,反应的Cu为0.1mol,其质量为6.4g;
故答案为:Cu;6.4;
(3)铝片和铜片插入浓HNO3溶液中,金属铝会钝化,金属铜和浓硝酸之间会发生自发的氧化还原反应,此时金属铜时负极,金属铝是正极;
插入稀NaOH溶液中,金属铜和它不反应,金属铝能和氢氧化钠发生自发的氧化还原反应,此时金属铝是负极,金属铜是正极;
故答案为:B;
(4)①氢氧燃料电池的正极是氧气得电子发生还原反应,电解质是酸性环境,所以电极反应式为:O2+4H++4e-=2H2O,
故答案为:O2+4H++4e-=2H2O;
②已知氢氧燃料电池的总反应为:2H2+O2=2H2O,电池工作一段时间后,生成水使溶液体积增大,则硫酸的浓度减小;
故答案为:减小.
点评 本题考查了原电池原理的应用,涉及电极判断与电极反应式书写等问题,做题时注意从氧化还原的角度判断原电池的正负极.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 制氧气时,用Na2O2或H2O2做反应物可选择相同的气体发生装置 | |
| B. | 制氯气时,用饱和NaHCO3和浓硫酸净化气体 | |
| C. | 制氨气时,用排水法或向上排空气法收集气体 | |
| D. | 制二氧化氮时,用水或NaOH溶液吸收尾气 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al元素最高化合价依次升高 | |
| B. | P、Cl最高价氧化物对应的水化物酸性增强 | |
| C. | N、O、F元素非金属性依次减弱 | |
| D. | Li、Na、K原子的电子层数依次增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
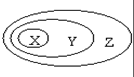 表中所示物质或概念间的从属关系符合右图的是( )
表中所示物质或概念间的从属关系符合右图的是( )| X | Y | Z | |
| A | 钠元素 | 主族元素 | 短周期元素 |
| B | 非电解质 | 化合物 | 纯净物 |
| C | 氯化铁 | 胶体 | 分散系 |
| D | 置换反应 | 氧化还原反应 | 放热反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
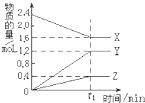 I.某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示:
I.某温度下,在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t1min时到达平衡,依图所示: 3Y+Z.
3Y+Z.查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com