
| A. | 将铜粉与硫粉混合均匀加热以制取CuS | |
| B. | 将铜丝插入浓硫酸中并加热,反应后再加水以观察CuSO4溶液的颜色 | |
| C. | 向CuSO4溶液中加入过量的NaOH溶液,过滤洗涤并收集沉淀充分灼烧以制取CuO | |
| D. | 向淀粉溶液中加入适量稀硫酸微热,再加少量新制Cu(OH)2并加热,产生砖红色沉淀 |
分析 A.S具有弱氧化性,与Cu反应生成低价金属硫化物;
B.铜丝插入浓硫酸中并加热,生成硫酸铜,硫酸铜溶液为蓝色;
C.CuSO4溶液中加入过量的NaOH溶液,生成氢氧化铜沉淀,灼烧分解生成CuO;
D.淀粉水解生成葡萄糖,检验葡萄糖在碱性条件下.
解答 解:A.S具有弱氧化性,将铜粉与硫粉混合均匀加热以制取Cu2S,故A错误;
B.铜丝插入浓硫酸中并加热,生成硫酸铜,硫酸铜溶液为蓝色,则反应后再加水以观察CuSO4溶液的颜色,故B正确;
C.CuSO4溶液中加入过量的NaOH溶液,生成氢氧化铜沉淀,灼烧分解生成CuO,则过滤洗涤并收集沉淀充分灼烧以制取CuO,故C正确;
D.淀粉水解生成葡萄糖,检验葡萄糖在碱性条件下,则水解后先加碱至碱性,再加少量新制Cu(OH)2并加热,产生砖红色沉淀,故D错误;
故选BC.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、发生的反应、物质的检验为解答的关键,侧重分析与实验能力的考查,注意元素化合物知识与实验的结合及实验的评价性分析,题目难度不大.


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜与盐酸反应:Cu+2H+═Cu2++H2↑ | |
| B. | 氧化铁与稀盐酸反应:Fe2O3+6H+═2Fe3++3H2O | |
| C. | 锌与硝酸银溶液反应:Zn+Ag+═Zn2++Ag | |
| D. | 在硫酸溶液中加入氢氧化钡溶液:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色透明的溶液中:Na+、SO42-、MnO4-、NO3- | |
| B. | 使无色酚酞试液呈红色的溶液中:Na+、Cu2+、SO42-、Cl- | |
| C. | pH=1的溶液中:K+、ClO-、S2-、Cl- | |
| D. | 弱碱性的溶液中:Na+、K+、HCO3-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向AgI中加一定浓度、一定体积的NaCl溶液,AgI可转化为AgCl | |
| B. | 常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度应该大于$\frac{1}{\sqrt{1.8}}$×10-11mol/L | |
| C. | AgI比AgCl更难溶于水,AgCl可以转化为AgI | |
| D. | 向c(Ag+)=1.8×10-4mol/L的溶液中加入等体积NaCl溶液,开始出现AgCl沉淀,则NaCl溶液浓度应大于1.0×10-6mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

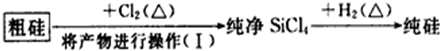
| 物质 | Si | SiCl4 |
| 沸点/℃ | 2355 | 57.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com