
关于铅蓄电池的说法正确的是()
A. 在放电时,正极发生的反应是Pb(s)+SO42﹣(aq)﹣2e﹣=PbSO4(s)
B. 在放电时,该电池的负极材料是铅板
C. 在充电时,电池中硫酸的浓度不断变小
D. 在充电时,阳极发生的反应是P bSO4(s)+2e﹣=Pb(s)+SO42﹣(aq)
bSO4(s)+2e﹣=Pb(s)+SO42﹣(aq)
考点: 常见化学电源的种类及其工作原理.
专题: 电化学专题.
分析: 由铅蓄电池的总反应PbO2+2H2SO4+Pb═2PbSO4+2H2O可知,放电时,Pb被氧化,应为电池负极反应,
电极反应式为Pb﹣2e﹣+SO42﹣=PbSO4,逆反应过程应该是充电时的阴极反应,正极上PbO2得电子被还原,
电极反应式为PbO2+SO42﹣+2e﹣+4H+═PbSO4+2H2O,逆反应应该是充电时的阳极反应.
解答: 解:A.铅蓄电池放电时,正极上PbO2得电子被还原,电极反应式为PbO2+SO42﹣+2e﹣+4H+═PbSO4+2H2O,故A错误;
B、由铅蓄电池的总反应PbO2+2H2SO4+Pb 2PbSO4+2H2O可知,放电时,Pb被氧化,应为电池负极,故B正确;
2PbSO4+2H2O可知,放电时,Pb被氧化,应为电池负极,故B正确;
C、由铅蓄电池的总反应PbO2+2H2SO4+Pb 2PbSO4+2H2O可知,充电时,会生成硫酸,电池中硫酸的浓度会增大,故C错误;
2PbSO4+2H2O可知,充电时,会生成硫酸,电池中硫酸的浓度会增大,故C错误;
D、由铅蓄电池的总反应PbO2+2H2SO4+Pb 2PbSO4+2H2O可知,充电时,阳极发生的反应是PbSO4+2H2O=PbO2+SO42﹣+2e﹣+
2PbSO4+2H2O可知,充电时,阳极发生的反应是PbSO4+2H2O=PbO2+SO42﹣+2e﹣+
4H+,故D错误.
故选B.
点评: 题考查原电池的工作原理,题目难度中等,本题注意电极反应式的书写,为解答该题的关键.


 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
下列有关实验的做法错误的是()
A. 用四氯化碳萃取溴水中的溴后,分液时,有机层应从分液漏斗的上口倒出
B. 检验NH4+时,向试样中加入NaOH溶液,微热,用湿润的红色石蕊试纸检验逸出的气体
C. 通过分液漏斗滴加溶液时,应打开上口的玻璃塞或将玻璃塞上的凹槽对准口颈部的小孔
D. 玻璃仪器洗涤干净的标准是:附着在仪器内壁上的水既不聚集成滴,也不成股流下
查看答案和解析>>
科目:高中化学 来源: 题型:
制备氯化物时,常用两种方法:①用金属与氯气直接化合制得;②用金属与盐酸反应制得.用以上两种方法都可制得的氯化物是()
A. AlCl3 B. FeCl3 C. FeCl2 D. CuCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
将Mg条、Al条平行插入一定浓度的NaOH溶液中,用导线、电流计连接成原电池,此电池工作时,下列叙述中正确的是()
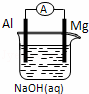
A. Mg比Al活泼,Mg 失去电子被氧化成Mg2+
B. 负极反应式为:Al+4OH﹣﹣3e﹣=AlO2﹣+2H2O
C. 该电池的内外电路中,电流均是由电子定向移动形成的
D. Al是电池阴极,开始工作时溶液中会立即有白色沉淀析出
查看答案和解析>>
科目:高中化学 来源: 题型:
Mg﹣AgCl电池是一种能被海水激活的一次性贮备电池,电池反应方程式为:2AgCl+Mg=Mg2++2Ag+2Cl﹣.有关该电池的说法正确的是()
A. Mg为电池的正极 B. 负极反应为AgCl+e﹣=Ag+Cl﹣
C. 不能被KCl 溶液激活 D. 可用于海上应急照明供电
查看答案和解析>>
科目:高中化学 来源: 题型:
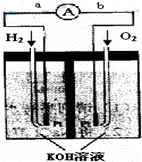
氢氧燃料电池是符合绿色化学理念的新型发电装置.下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b 表示).
(2)负极反应式为 .
(3)电极表面镀铂粉的原因为增
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能.因此,大量安全储氢是关键技术之一.金属锂是一种重要的储氢材料,吸氢和放氢原理如下:Ⅰ.2Li+H2 2LiHⅡ.LiH+H2O═LiOH+H2↑
2LiHⅡ.LiH+H2O═LiOH+H2↑
①反应Ⅰ中的还原剂是Li,反应Ⅱ中的氧化剂是H2O.
②用锂吸收224L(标准状况)H2,再由生成的LiH与H2O作用放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 .
③若改用熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极.已知负极的电极反应是CH4+4CO32﹣﹣8e﹣=5CO2+2H2O.则正极的电极反应是 .为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,此电池工作时必须有部分A物质参加循环,则A物质的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,某密闭容器中发生反应:N2(g)+3H2(g)═2NH3(g).反应物N2的浓度10s内从2mol/L降为1mol/L,在这段时间内用N2浓度的变化表示的反应速率为( )
A. 0.05 mol/(L•s) B. 0.1 mol/(L•s) C. 0.15 mol/(L•s) D. 0.2 mol/(L•s)
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的一个原子形成的离子可表示为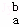 Xn﹣,下列说法正确的是( )
Xn﹣,下列说法正确的是( )
A. 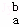 Xn﹣含有的中子数为a+b
Xn﹣含有的中子数为a+b
B. 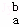 Xn﹣含有的电子数为a﹣n
Xn﹣含有的电子数为a﹣n
C. X原子的质量数为a+b+n
D. 一个X原子的质量约为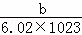 g
g
查看答案和解析>>
科目:高中化学 来源: 题型:
依据事实,写出下列反应的热化学方程式.
(1)1molN2(g)与适量O2(g)反应生成NO2(g),吸收68kJ热量: ;
(2)1molCu(s)与适量O2(g)反应生成CuO(s),放出157kJ热量: ;
(3)卫星发射时可用肼(N2H4)作燃料,1mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(l),放出622kJ热量:
(4)10g C2H6(g)完全燃烧生成CO2(g)和H2O(l),放出a kJ热量,写出表示C2H6燃烧热的热化学方程式:
(5)已知:WO2(s)+2H2(g)═W(s)+2H2O(g)△H=+66.0kJ/mol;WO2(g)+2H2(g)═W(s)+2H2O(g)△H=﹣137.9kJ/mol.则WO2(s)═WO2(g)的△H=
(6)已知:Al2O3(s)+AlCl3(g)+3C(s)═3AlCl(g)+3CO(g)△H=a kJ/mol,2Al(l)+AlCl3(g)═3AlCl(g)△H=b kJ/mol,则反应Al2O3(s)+3C(s)═2Al(l)+3CO(g)的△H= J/mol(用含a、b的代数式表示).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com