
【题目】下列离子中,电子数大于质子数,且质子数大于中子数的是( )
A. 16OH﹣ B. Mg2+ C. 16OD﹣ D. D316O+
科目:高中化学 来源: 题型:
【题目】下列除去括号内杂质的方法正确的是( )
A.FeCl2(FeCl3):加入足量铁屑,充分反应后过滤
B.CO2(HCl):通过饱和NaOH溶液,收集气体
C.N2(O2):通过灼热的CuO粉末,收集气体
D.KCl (MgCl2):加入适量NaOH溶液,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的NaOH固体中加入由硫酸铜和硫酸组成的混合物的溶液,充分搅拌,恰好完全反应,有蓝色沉淀生成,过滤,所得滤液的质量与加入的原混合物溶液的质量相等.则与硫酸铜反应的氢氧化钠和与硫酸反应的氢氧化钠的物质的量之比为?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaBH4( 硼氢化钠)广泛用于贮氢、有机合成及纳米材料制取等。回答下列问题:
(1)NaBH4的电子式为_________。
(2) NaBH4水解生成H2同时生成NaBO2,每生成1mol H2 转移电子数为______个;Kreevoy 等提出在碱性溶液中该水解反应的半衰期t1/2(反应物浓度减少一半所需时间) 与温度的关系式为l gt1/2=pH-(0.034T-1.92),其他条件相同时,贮氢时为减慢水解速率,应控制pH 及T的条件是______;已知0℃、pH=10时半衰期为4.32×102min,若此时NaBH4的依度为4.32 molL.1,则t0至半衰期生成H2的平均速率为_________molL-1min-1。
(3)直接NaBH4碱性燃料电池的结构如下图所示:
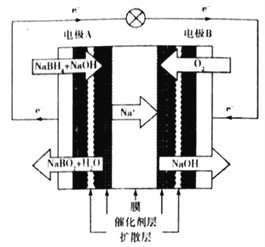
电池工作时,电极B周围溶液的pH______ (填“升高”“降低”或“不变”),电极A 上发生的电极反应式为_________________。
(4)制取NaBH4的方法之一是将Na2B4O7、SiO2 及金属Na按一定比例混合通H2 并加热到360- 370 ℃(同时生成Na2SiO3),该反应的化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作中最终可以得到氢氧化铝的是
A. 氧化铝与水混合加热
B. 金属铝与水反应
C. 过量的烧碱溶液加入到氯化铝溶液中
D. 过量的氨气通入到氯化铝溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2(g)+I2(g)2HI(g)已经达到平衡状态的标志是( )
①c(H2)=c(I2)=c(HI)
②c(H2):c(I2):c(HI)=1:1:2
③c(H2)、c(I2)、c(HI)不再随时间而改变
④单位时间内生成nmolH2的同时生成2nmolHI
⑤单位时间内生成n mol H2的同时生成n mol I2
⑥反应速率v(H2)=v(I2)= ![]() v(HI)
v(HI)
⑦一个H﹣H键断裂的同时有两个H﹣I键断裂
⑧温度和体积一定时,容器内压强不再变化
⑨温度和体积一定时,混合气体的颜色不再变化
⑩温度和压强一定时,混合气体的密度不再变化
条件一定,混合气体的平均相对分子质量不再变化.
A.5项
B.4项
C.3项
D.2项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的NaOH 溶液中逐滴加入AlCl3溶液,生成沉淀A1(OH)3的量随AlCl3加入量的变化关系如右图所示。则下列离子组在对应的溶液中一定能大量共存的是
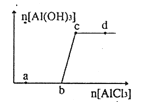
A. a点对应的溶液中:Na+、Fe3+、SO42-、HCO3-
B. b点对应的溶液中:Na+、S2-、SO42-、Cl-
C. c点对应的溶液中:Ag+、Ca2+、NO3-、F-
D. d点对应的溶液中:K+、NH4+、I-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用所学化学知识解答问题:
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,则该反应的热化学方程式应为
(2)已知下列各物质的键能:N≡N 946kJ/mol、H﹣H 436kJ/mol、N﹣H 391kJ/mol,写出合成氨的热化学方程式为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com