
【题目】(1)下图是等质量的碳酸钠、碳酸氢钠粉末分别与足量的盐酸发生反应时的情景,产生二氧化碳气体的体积较多的试管中加入的固体试剂是________,当反应结束时,A、B中消耗的盐酸的质量之比为________。

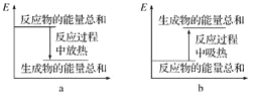
(2)实验过程中我们还能感受到碳酸钠与盐酸反应时是放热反应,而碳酸氢钠与盐酸反应时表现为吸热。在A、B试管的反应过程中,反应体系的能量变化的总趋势分别对应于A为________,B为________(填“a”或“b”)。
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案科目:高中化学 来源: 题型:
【题目】氨的化合物在生产、生活中广泛存在。
(1)我国长征系列运载火箭用肼(N2H4)作燃料。N2H4与NH3有相似的化学性质。
①写出肼与盐酸反应的离子方程式:_______________________________。
②在火箭推进器中装有液态肼和双氧水,当它们混合时迅速反应生成氮气和水蒸气,写出反应的化学方程式:_____________________________________。
③火箭发射时以肼为燃料,也可以用一氧化氮作氧化剂,反应过程中若转移2mol电子则消耗燃料肼的质量为______________。
(2)汽车尾气中的氮氧化物是形成酸雨、酸雾的有毒气体之一,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。

写出净化过程中总反应的化学方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表短周期的一部分:
① | ||||||||
⑨ | ② | ③ | ④ | |||||
⑤ | ⑥ | ⑦ | ⑧ | |||||
(1) ①-⑦元素中非金属性最强的元素位于周期表中的位置为______________________。
(2) ③与⑤形成的化合物与水反应产生气体,该反应的化学方程式 _______________ 。该化合物的电子式为______
(3) ④所形成的单质与水反应的方程式 _____________。
(4) ②、③、⑨的最高价含氧酸的酸性由弱到强的顺序是__________________(用化学式表示)。
(5) 表中元素⑤和⑥的最高价氧化物的水化物之间相互反应的离子方程式为____________。
(6) ②的气态氢化物的实验室制法的反应原理:____________________;(写出化学方程式)
②的气态氢化物和它的最高价氧化物的水化物反应的产物为______________(“离子”或“共价”)化合物。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验现象一定能得出相应结论的是
选项 | A | B | C | D |
装置图 |
|
|
|
|
现象 | 右边试管产生气泡较快 | 左边棉球变棕黄色,右边棉球变蓝色 | 试管中先出现淡黄色固体,后出现黄色固体 | 试管中液体变浑浊 |
结论 | 催化活性:Fe3+>Cu2+ | 氧化性:Br2>I2 | Ksp:AgCl>AgBr>AgI | 非金属性:C>Si |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”表示,如:可简写为![]() ,有机物X的键线式为
,有机物X的键线式为 ,下列说法不正确的是
,下列说法不正确的是
A. X的化学式为C8H8
B. Y是X的同分异构体,且属于芳香烃,则Y的结构简式可以为![]()
C. X能使酸性高锰酸钾溶液褪色
D. X与足量的氢气在一定条件下反应生成环状饱和烃的一氯代物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇分子中各化学键如图所示.下列关于乙醇在不同的反应中断裂化学键的说法错误的是
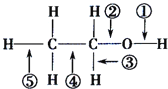
A. 与金属钠反应时,键①断裂
B. 在加热和Cu催化下与O2反应时,键①、③断裂
C. 与浓硫酸共热发生消去反应时,键②③断裂
D. 与乙酸、浓硫酸共热发生酯化反应时,键①断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】正确掌握化学用语是学好化学的基础.下列化学用语中不正确的是( )
A. 乙烯的结构简式CH2=CH2 B. CH4分子的球棍模型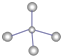
C. Ca2+的结构示意图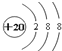 D. 乙醇的分子式C2H6O
D. 乙醇的分子式C2H6O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CoCl2·6H2O是一种饲料营养强化剂。一种利用水钴矿(主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等)制取CoCl2·6H2O的工艺流程如下:
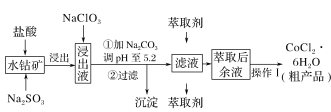
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl2·6H2O熔点为86 ℃,加热至110~120 ℃时,失去结晶水生成无水氯化钴。
(1)写出浸出过程Co2O3发生反应的离子方程式:______________。
(2)写出NaClO3发生反应的主要离子方程式:_____________;
(3)“加Na2CO3调pH至5.2”,过滤所得到的沉淀成分为________。
(4)“操作1”中包含3个基本实验操作,它们依次是_________、_________和过滤。
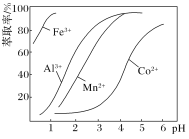
(5)萃取剂对金属离子的萃取率与pH的关系如图。向“滤液”中加入萃取剂的目的是____________;萃取剂使用的最佳pH范围是_____(填代号)。
A.2.0~2.5 B.3.0~3.5
C.4.0~4.5 D.5.0~5.51
(6)为测定粗产品中CoCl2·6H2O的含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量。通过计算发现粗产品中CoCl2·6H2O的质量分数大于100%,其原因可能是________________________。(答一条即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com