
 金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如图所示:
金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如图所示:分析 (1)图象分析金刚石能量高于石墨,能量越低越稳定,所以说明石墨稳定,图象分析1mol石墨完全燃烧生成1mol二氧化碳放出的热量为393.5kJ,则石墨的燃烧热为△H=-393.5kJ?mol-1;
(2)(2)Fe2O3(s)+$\frac{3}{2}$C(s)═$\frac{3}{2}$CO2(g)+2Fe(s)△H=+234.1kJ/mol
②C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
由盖斯定律-②×$\frac{3}{2}$+①得:Fe2O3(s)═2Fe(s)+$\frac{3}{2}$O2(g)△H=-(-393.5kJ•mol-1)×$\frac{3}{2}$+234.1kJ•mol-1;
(3)24g石墨物质的量为2mol,在一定量空气中燃烧,依据元素守恒,若生成二氧化碳质量为88g,若生成一氧化碳质量为56g,生成气体72g,56g<72g<88g,判断生成的气体为一氧化碳和二氧化碳气体,设一氧化碳物质的量为x,二氧化碳物质的量为(2-x)mol,28x+44(2-x)=72g,x=1mol,二氧化碳物质的量为1mol.
解答 解:(1)金刚石能量高于石墨,所以等物质的量的金刚石和石墨完全燃烧,金刚石放出热量多;能量越低越稳定,所以说明石墨稳定,石墨的燃烧热为△H=-393.5kJ?mol-1,所以石墨燃烧热的热化学方程式为:C(s,石墨)+O2(g)═CO2(g)△H=-393.5kJ?mol-1,
故答案为:金刚石;石墨;C(s,石墨)+O2(g)═CO2(g)△H=-393.5kJ?mol-1;
(2)Fe2O3(s)+$\frac{3}{2}$C(s)═$\frac{3}{2}$CO2(g)+2Fe(s)△H=+234.1kJ/mol
②C(s)+O2(g)═CO2(g)△H=-393.5kJ/mol
由盖斯定律-②×$\frac{3}{2}$+①得:Fe2O3(s)═2Fe(s)+$\frac{3}{2}$O2(g)△H=-(-393.5kJ•mol-1)×$\frac{3}{2}$+234.1kJ•mol-1
即Fe2O3(s)═2Fe(s)+$\frac{3}{2}$O2(g)△H=+824.4kJ•mol-1,
故答案为:+824.4;
(3)24g石墨物质的量为2mol,在一定量空气中燃烧,依据元素守恒,若生成二氧化碳质量为88g,若生成一氧化碳质量为56g,生成气体72g,56g<72g<88g,判断生成的气体为一氧化碳和二氧化碳气体,设一氧化碳物质的量为x,二氧化碳物质的量为(2-x)mol,28x+44(2-x)=72g,x=1mol,二氧化碳物质的量为1mol;依据图象可知C(石墨,s)+O2(g)═CO2(g)△H=-393.5 kJ•mol-1 、C(石墨,s)+$\frac{1}{2}$O2(g)═CO(g)△H=-110.5 kJ•mol-1 ,生成二氧化碳和一氧化碳混合气体放出热量=393.5 kJ•mol-1 ×1mol+110.5 kJ•mol-1 ×1mol=504KJ,故答案为:504.0.
点评 本题考查了化学反应能量变化的图象分析计算,热化学方程式的书写方法,掌握基础是关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ② | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2O | B. | NO | C. | NH4NO3 | D. | N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加聚反应也可能有水生成 | |
| B. | 水、乙醇、氢氧化钠中都存在羟基 | |
| C. | 王水、溴水、水银、水晶中均含有“H2O” | |
| D. | 在某些有机反应中,水可能是反应物也可能是生成物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 500 mL容量瓶 | B. | 胶头滴管 | C. | 试管 | D. | 托盘天平 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在热化学方程式中,物质化学式前面的化学计量数可以为整数也可以为简单分数 | |
| B. | 同一化学反应,热化学方程式中物质的化学计量数不同,反应的△H也不同 | |
| C. | 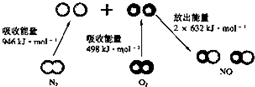 N2(g)与O2(g)反应生成NO(g)过程中的能量变化如图所示,若加入催化剂,化学反应速率改变,△H也改变 N2(g)与O2(g)反应生成NO(g)过程中的能量变化如图所示,若加入催化剂,化学反应速率改变,△H也改变 | |
| D. | 化学反应中化学键的断裂和形成是反应过程中有能量变化的本质原因 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com