
”¾ĢāÄæ”æ£Ø1£©ŌŚŅ»¶ØĢõ¼žĻĀ£¬½«1.00molN2£Øg£©Óė3.00molH2£Øg£©»ģŗĻÓŚŅ»øö10.0LĆܱÕČŻĘ÷ÖŠ£¬ŌŚ²»Ķ¬ĪĀ¶ČĻĀ“ļµ½Ę½ŗāŹ±NH3£Øg£©µÄĘ½ŗāÅضČČēĶ¼1ĖłŹ¾”£ĘäÖŠĪĀ¶ČĪŖT1Ź±Ę½ŗā»ģŗĻĘųĢåÖŠ°±ĘųµÄĢå»ż·ÖŹżĪŖ25.0%”£
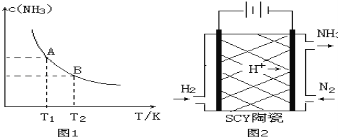
µ±ĪĀ¶ČÓÉT1±ä»Æµ½T2Ź±£¬Ę½ŗā³£Źż¹ŲĻµK1 K2£ØĢī”°£¾”±£¬”°£¼”±»ņ”°=”±£©”£
¢ŚøĆ·“Ó¦ŌŚT1ĪĀ¶ČĻĀ5.00min“ļµ½Ę½ŗā£¬Õā¶ĪŹ±¼äÄŚN2µÄ»Æѧ·“Ó¦ĖŁĀŹĪŖ ”£
¢ŪT1ĪĀ¶ČĻĀøĆ·“Ó¦µÄ»ÆŃ§Ę½ŗā³£ŹżK1= ”£
£Ø2£©øł¾Ż×īŠĀ”°ČĖ¹¤¹ĢµŖ”±µÄŃŠ¾æ±ØµĄ£¬ŌŚ³£ĪĀ³£Ń¹ŗĶ¹āÕÕĢõ¼žĻĀN2ŌŚ“߻ƼĮ±ķĆęÓėĖ®·¢Éś·“Ó¦£ŗ2N2£Øg£©+6H2O£Øl£©=4NH3£Øg£©+3O2£Øg£©£¬“Ė·“Ó¦µÄ”÷S 0£ØĢī”°£¾”±»ņ”°£¼”±£©”£
ČōN2£Øg£©+3H2£Øg£©=2NH3£Øg£© ”÷H=a kJ/mol
2H2£Øg£©+O2£Øg£©=2H2O£Øl£© ”÷H=b kJ/mol
2N2£Øg£©+6H2O£Øl£©=4NH3£Øg£©+3O2£Øg£©µÄ”÷H= £ØÓĆŗ¬a”¢bµÄŹ½×Ó±ķŹ¾£©”£
£Ø3£©æĘѧ¼Ņ²ÉÓĆÖŹ×Óøßµ¼µēŠŌµÄSCYĢÕ“É£ØæÉ“«µŻH+£©ŹµĻÖĮĖµĶĪĀ³£Ń¹ĻĀøß×Ŗ»ÆĀŹµÄµē»ÆѧŗĻ³É°±£¬Ę䏵ŃéŌĄķŹ¾ŅāĶ¼ČēĶ¼2ĖłŹ¾£¬ŌņŅõ¼«µÄµē¼«·“Ó¦Ź½ŹĒ ”£
£Ø4£©ŅŃÖŖijŠ©Čõµē½āÖŹŌŚĖ®ÖŠµÄµēĄėĘ½ŗā³£Źż£Ø25”ę£©ČēĻĀ±ķ£ŗ
Čõµē½āÖŹ | H2CO3 | NH3.H2O |
µēĄėĘ½ŗā³£Źż | Ka1=4.30”Į10-7 Ka2=5.61”Į10-11 | Kb=1.77”Į10-5 |
ĻÖÓŠ³£ĪĀĻĀ0£®1 mol”¤L-1µÄ£ØNH4£©2CO3ČÜŅŗ£¬
¢ŁøĆČÜŅŗ³Ź ŠŌ£ØĢī”°Ėį”±”¢”°ÖŠ”±”¢”°¼ī”±£©£¬ŌŅņŹĒ ”£
¢ŚøĆ£ØNH4£©2CO3ČÜŅŗÖŠø÷Ī¢Į£ÅضČÖ®¼äµÄ¹ŲĻµŹ½²»ÕżČ·µÄŹĒ ”£
A£®c£ØNH4+£©>c£ØCO32-£©>c£ØHCO3-£©>c£ØNH3.H2O£©
B£®c£ØNH4+£©+c£ØH+£©=c£ØHCO3-£©+c£ØOH-£©+c£ØCO32-£©
C£®c£ØCO32-£©+c£ØHCO3-£©+c£ØH2CO3£©=0.1mol/L
D£®c£ØNH4+£©+c£ØNH3.H2O£©=2c£ØCO32-£©+2c£ØHCO3-£©+2c£ØH2CO3£©
E£®c£ØH+£©+c£ØHCO3-£©+c£ØH2CO3£©=c£ØOH-£©+c£ØNH3.H2O£©
”¾“š°ø”æ£Ø1£©¢Ł£¾£»¢Ś8.00”Į10©3mol/£ØLmin£©£»¢ŪK1”Ö18.3£»
£Ø2£©£¾£¬£Ø2a©3b£©kJ/mol£»£Ø3£©N2+6e©+6H+=2NH3£»
£Ø4£©¢Ł¼ī£¬ÓÉÓŚNH3”¤H2OµÄµēĄėĘ½ŗā³£Źż“óÓŚHCO3-µÄµēĄėĘ½ŗā³£Źż£¬Ņņ“ĖCO32-Ė®½ā³Ģ¶Č“óÓŚNH4+Ė®½ā³Ģ¶Č£¬ČÜŅŗ³Ź¼īŠŌ£»¢Ś BE”£
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©¢Łøł¾ŻĶ¼1£¬Ėę×ÅĪĀ¶ČµÄÉżøߣ¬NH3µÄÅØ¶Č½µµĶ£¬øł¾ŻĄÕĻÄĢŲĮŠŌĄķ£¬Õż·“Ó¦·½ĻņŹĒ·ÅČČ·“Ó¦£¬»ÆŃ§Ę½ŗā³£ŹżŹÜĪĀ¶ČµÄÓ°Ļģ£¬ÉżøßĪĀ¶Č£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬»ÆŃ§Ę½ŗā³£Źż½µµĶ£¬¼“K1>K2£»
¢Ś N2£«3H2![]() 2NH3
2NH3
ĘšŹ¼£ŗ 1 3 0
±ä»Æ£ŗ x 3x 2x
Ę½ŗā£ŗ1£x 3£3x 2x
2x/£Ø4£2x£©”Į100%=25%£¬½āµĆx=0.4£¬øł¾Ż»Æѧ·“Ó¦ĖŁĀŹµÄ¶ØŅ壬v£ØN2£©=0.4/£Ø10”Į5£©mol/£ØL”¤min£©=8.00”Į10©3mol/£ØLmin£©£»¢Ūøł¾Ż»ÆŃ§Ę½ŗā³£ŹżµÄ±ķ“ļŹ½£¬K=c2£ØNH3£©/[c£ØN2£©”Įc3£ØH2£©]”Ö18.3£»£Ø2£©¹ĢĢ¬”śŅŗĢå”śĘųĢ壬»ģĀŅ¶ČŌö“ó£¬ŹĒģŲŌö£¬·“Ó¦ŗóĘųĢåĻµŹżÖ®ŗĶ“óÓŚ·“Ó¦Ē°£¬Ņņ“Ė“Ė·“Ó¦ŹĒ·½³ĢŹ½ŹĒ”÷S>0£»¢ŁN2£Øg£©+3H2£Øg£©=2NH3£Øg£©£¬¢Ś2H2£Øg£©+O2£Øg£©=2H2O£Øl£©£¬2”Į¢Ł£3”Į¢ŚµĆ³ö”÷H=£Ø2a£3b£©kJ”¤mol£1£»£Ø3£©½ÓµēŌ“Õż¼«µÄŅ»¼«ĪŖŃō¼«£¬½ÓµēŌ“øŗ¼«µÄŅ»¼«ĪŖŅõ¼«£¬ŗĻ³É°±ÖŠµŖĘų»ÆŗĻ¼Ū½µµĶ£¬ŌŚŅõ¼«ÉĻµĆµ½µē×Ó£¬øł¾Ż½į¹¹Ź¾ŅāĶ¼£¬»·¾³ŹĒĖįŠŌ£¬Ņņ“Ėµē¼«·“Ó¦Ź½ĪŖ£ŗN2+6e©+6H+=2NH3£»£Ø4£©¢Łøł¾ŻµēĄėĘ½ŗā³£Źż£¬æÉŅŌ·¢ĻÖNH3”¤H2OµÄµēĄėĘ½ŗā³£Źż“óÓŚHCO3£µÄµēĄėĘ½ŗā³£Źż£¬ŃĪĄąĖ®½ā¹ęĀÉŌ½ČõŌ½Ė®½ā£¬CO32£µÄĖ®½ā³Ģ¶Č“óÓŚNH4£«µÄĖ®½ā£¬Ņņ“ĖĢ¼Ėįļ§µÄĖ®ČÜŅŗĻŌ¼īŠŌ£»¢ŚA”¢CO32£µÄĖ®½ā³Ģ¶Č“óÓŚNH4£«µÄĖ®½ā£¬¼“ÅØ¶Č“óŠ”ŹĒc£ØNH4£«£©>c£ØCO32££©>c£ØHCO3££©>c£ØNH3”¤H2O£©£¬¹ŹĖµ·ØÕżČ·£»B”¢øł¾ŻµēŗÉŹŲŗć£¬Ó¦ŹĒ£ŗc£ØNH4£«£©+c£ØH£«£© = c£ØHCO3££©+c£ØOH££©+2c£ØCO32££©£¬¹ŹĖµ·Ø“ķĪó£»C”¢øł¾ŻĪļĮĻŹŲŗć£¬Ó¦ŹĒc£ØCO32££©+c£ØHCO3££©+c£ØH2CO3£© = 0.1mol”¤L£1£¬¹ŹĖµ·ØÕżČ·£»D”¢øł¾ŻĪļĮĻŹŲŗć£¬£®c£ØNH4£«£©+c£ØNH3.H2O£© = 2c£ØCO32££©+2c£ØHCO3££©+2c£ØH2CO3£©£¬¹ŹĖµ·ØÕżČ·£»E”¢øł¾ŻÖŹ×ÓŹŲŗć£¬c£ØH£«£©+c£ØHCO3££©+2c£ØH2CO3£© = c£ØOH££©+c£ØNH3”¤H2O£©£¬ ¹ŹĖµ·Ø“ķĪó”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŅĶ¼ŹĒ298K Ź±N2ÓėH2·“Ó¦¹ż³ĢÖŠÄÜĮæ±ä»ÆµÄĒśĻßĶ¼”£ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ( )
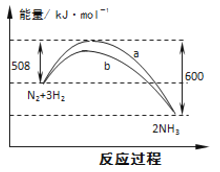
A£®øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗN2(g) + 3H2(g) ![]() 2NH3(g) ¦¤H = -92kJ”¤mol-1
2NH3(g) ¦¤H = -92kJ”¤mol-1
B£®bĒśĻߏĒ¼ÓČė“߻ƼĮŹ±µÄÄÜĮæ±ä»ÆĒśĻß
C£®¼ÓČė“߻ƼĮ, øĆ»Æѧ·“Ó¦µÄ»ī»ÆÄÜŗĶ·“Ó¦Čȶ¼øıä
D£®ŌŚĪĀ¶ČĢå»żŅ»¶ØµÄĢõ¼žĻĀ, ĶØČėlmol N2ŗĶ3molH2 ·“Ó¦ŗó·Å³öµÄČČĮæĪŖQ1kJ, ČōĶØČė2mol N2ŗĶ6mol H2 ·“Ó¦ŗó·Å³öµÄČČĮæĪŖQ2kJ Ōņ184>Q2 >2Q1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ŹĒÄ³Ń§Š£ŹµŃéŹŅĀņ»ŲµÄĮņĖįŹŌ¼Į±źĒ©µÄ²æ·ÖÄŚČŻ”£ÅŠ¶ĻĻĀĮŠĖµ·ØÕżČ·µÄŹĒ( )

A. øĆĮņĖįµÄÅضČĪŖ9.2 mol”¤L£1
B. ÅäÖĘ480 mL 4.6 mol”¤L£1µÄĻ”ĮņĖįŠčøĆH2SO4125mL
C. øĆĮņĖįÓėµČĢå»żĖ®»ģŗĻÖŹĮæ·ÖŹż±äĪŖ49%
D. Č”øĆĮņĖį100 mL£¬ŌņÅØ¶Č±äĪŖŌĄ“µÄ![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼øÖÖĪļÖŹµÄ»ÆѧŹ½¼°ĘäĆū³Ę·Ö±šŹĒ£ŗNa2S2O3Įņ“śĮņĖįÄĘ£»CaSx¶ąĮņ»ÆøĘ£»BaO2¹żŃõ»Æ±µ”£øł¾ŻÉĻŹöĆüĆū¹ęĀÉK2CS3µÄĆū³ĘÓ¦ĪŖ( )
A£®ČżĮņ“śĢ¼Ėį¼Ų B£®¶ąĮņĢ¼»ÆøĘ·Ź C£®¹żĮņĢ¼Ėį¼Ų D£®³¬ĮņĢ¼Ėį¼Ų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹ³Ę·øưܵÄŌŅņÖ®Ņ»ŹĒŅņĪŖÓŠŃõĘų“ęŌŚ¶ų·¢ÉśŃõ»Æ·“Ó¦”£Ņņ“Ė£¬ĪüŹÕµōĆÜ·āµÄŹ³Ę·°ü×°ŗŠÄŚµÄŃõĘų¾ĶæÉŅŌŃÓ³¤Ź³Ę·µÄ±£ÖŹĘŚ”£ĻĀĮŠÄÄÖÖĪļÖŹŹŹŅĖ·āČėŹ³Ę·°ü×°ŗŠÖŠÓĆĄ“ĪüŹÕµōŗŠÄŚµÄŃõĘų£¬ŃÓ³¤Ź³Ę·µÄ±£ÖŹĘŚµÄŹĒ( )
A£®ŗģĮ× B£®¹ĢĢåÉÕ¼ī C£®Ģś·Ū D£®ÉśŹÆ»Ņ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ 4Ęæ³£ÓĆČÜŅŗ£ŗ¢ŁBaCl2ČÜŅŗ£¬¢ŚNaCl ČÜŅŗ£¬¢ŪNa2SO4ČÜŅŗ£¬¢ÜCuSO4ČÜŅŗ”£²»ÓĆĘäĖūŹŌ¼Į£¬æÉĶعż ŹµŃé·½·Ø½«ĖüĆĒŅ»Ņ»¼ų±šæŖĄ“£¬¼ų±š³öĄ“µÄĻČŗóĖ³ŠņæÉÄÜŹĒ£Ø £©
A. ¢Ł¢Ü¢Ū¢Ś B. ¢Ł¢Ū¢Ü¢Ś C. ¢Ü¢Ł¢Ū¢Ś D. ¢Ü¢Ś¢Ł¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”放2016ÄźŠĀæĪ±ź1”æĻĀĮŠ¹ŲÓŚÓŠ»ś»ÆŗĻĪļµÄĖµ·ØÕżČ·µÄŹĒ
A£®2-¼×»ł¶”ĶéŅ²³ĘĪŖŅģ¶”Ķé
B£®ÓÉŅŅĻ©Éś³ÉŅŅ“¼ŹōÓŚ¼Ó³É·“Ó¦
C£®C4H9ClÓŠ3ÖÖĶ¬·ÖŅģ¹¹Ģå
D£®ÓĶÖ¬ŗĶµ°°×ÖŹ¶¼ŹōÓŚøß·Ö×Ó»ÆŗĻĪļ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚÉśĪļĢåµÄ×é³ÉŌŖĖŲµÄĖµ·Ø£¬ÕżČ·µÄŹĒ£Ø £©
A. Ö¬·¾”¢Į×Ö¬ŗĶµ°°×ÖŹ¶¼æÉŅŌ¹©ÄÜ
B. ĢĒĄą”¢Ö¬ÖŹŗĶµ°°×ÖŹ¶¼ŗ¬ÓŠC”¢H”¢OŌŖĖŲ
C. Š”ĀóĢåÄŚµÄ»ÆѧŌŖĖŲÓė×ŌČ»½ēÖŠµÄ»ÆѧŌŖĖŲŌŚÖÖĄąŗĶŗ¬ĮæÉĻ»ł±¾ĻąĶ¬
D. Š”ĀóĢåÄŚµÄ»ÆѧŌŖĖŲÓėÓńĆ×ĢåÄŚµÄ»ÆѧŌŖĖŲŌŚÖÖĄąŗĶŗ¬ĮæÉĻ»ł±¾ĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĻÖĻó²»ÄÜÓĆ”°ĻąĖĘĻąČÜ”± ¹ęĀɽāŹĶµÄŹĒ
A£®ĀČ»ÆĒāŅ×ČÜÓŚĖ® B£®ĀČĘųŅ×ČÜÓŚNaOHČÜŅŗ
C£®µāŅ×ČÜÓŚCCl D£®µāÄŃČÜÓŚĖ®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com