
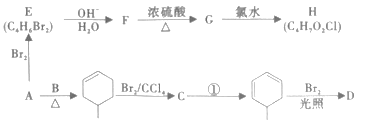
【题目】工业上用一种石油化工产品A(C4H6)为原料合成两种含卤素的有机化合物的合成路线如图。
已知:Ⅰ.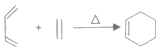 ;
;
II.E的核磁共振氢谱有两个吸收峰且能使溴的四氣化碳溶液褪色;
III.D分子不含甲基,G的分子式为C4H6O,且结构对称。
回答下列问题:
(1)A的系统命名为__,B的结构简式为__。
(2)A→E的反应类型为__,由G和氯水中的某一种成分发生加成反应生成H(不含经基)的化学方程式为__。
(3)下列有关说法正确的是__。
A.烃A的所有原子可能在同一平面上
B.G的一种同分异构体可能发生银镜反应
C.D的结构简式为![]()
D.将nmolA和nmolB通过加聚反应得到高聚物的聚合度为2n
(4)H的同分异构体中含有羧基的结构有__种,写出其中一种在核磁共振氢谱上有2组峰的有机物的结构简式__。
(5)结合上述合成路线中的信息写出以A和乙醇为起始原料合成氯环己烷的路线__。(无机原料自选)。
【答案】1,3-丁二烯 CH3CH=CH2 加成反应  AB 5 (CH3)2CClCOOH
AB 5 (CH3)2CClCOOH 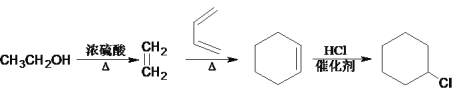
【解析】
根据流程图,A(C4H6)与溴加成生成E(C4H6Br2),E的核磁共振氢谱有2个吸收峰且能使溴的CCl4溶液褪色,E为CH2BrCH=CHCH2Br,则A为CH2=CH-CH=CH2。E在碱性溶液中水解生成F,F为二元醇,F为CH2OHCH=CHCH2OH,F在浓硫酸存在是加热,生成G,其分子式为C4H6O,可知G为![]() ,G和氯水中的HClO加成生成H,H分子不含羟基,只能为
,G和氯水中的HClO加成生成H,H分子不含羟基,只能为 ;根据信息Ⅰ,B为丙烯。
;根据信息Ⅰ,B为丙烯。 与溴发生加成反应生成C,C为
与溴发生加成反应生成C,C为 ,C发生卤代烃的消去反应,生成
,C发生卤代烃的消去反应,生成 ,
, 与溴在光照时发生取代反应,生成D,D中不含甲基,说明溴原子是取代甲基上的H原子,则D为
与溴在光照时发生取代反应,生成D,D中不含甲基,说明溴原子是取代甲基上的H原子,则D为 。
。
(1)根据分析,A为CH2=CH-CH=CH2,A的系统命名为1,3-丁二烯;B为丙烯,其结构简式为CH3CH=CH2;
(2)A到E发生的是1,3-丁二烯和溴的加成反应;根据H的结构可知,G和次氯酸发生加成反应生成H,根据上面分析,可写出化学方程式: ;
;
(3)A.烃A为1,3-丁二烯,碳碳双键以及与碳碳双键的碳原子相连的原子均在同一个平面上,中间的碳碳单键可以旋转,因此分子内所有原子可能共平面,A正确;
B.G的结构简式为![]() ,其分子式为C4H6O,分子中可能含有醛基,故可能发生银镜反应,B正确;
,其分子式为C4H6O,分子中可能含有醛基,故可能发生银镜反应,B正确;
C. 与溴在光照时发生取代反应,生成D,D中不含甲基,说明溴原子是取代甲基上的H原子,则D为
与溴在光照时发生取代反应,生成D,D中不含甲基,说明溴原子是取代甲基上的H原子,则D为 ,不可能为
,不可能为 ,C错误;
,C错误;
D.将nmolA和nmolB通过家具反应得到高聚物的聚合度为n,D错误;
答案选AB;
(4)H为 ,H的同分异构体中含有羧基,CH2ClCH2CH2COOH,CH3CHClCH2COOH、CH3CH2CHClCOOH、CH3)2CClCOOH、CH2ClCH(CH3)COOH,共5种;其中一种在核磁共振氢谱上有2组峰的有机物为(CH3)2CClCOOH;
,H的同分异构体中含有羧基,CH2ClCH2CH2COOH,CH3CHClCH2COOH、CH3CH2CHClCOOH、CH3)2CClCOOH、CH2ClCH(CH3)COOH,共5种;其中一种在核磁共振氢谱上有2组峰的有机物为(CH3)2CClCOOH;
(5)以A(1,3-丁二烯)和乙醇为起始原料合成一氯环己烷。要合成一氯环己烷,可以先合成环己烯,可以用1,3-丁二烯和乙烯合成环己烯,制备乙烯,只需要将乙醇中的羟基消去即可,则合成路线为 。
。


科目:高中化学 来源: 题型:
【题目】意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子。N4分子结构如图所示,下列说法正确的是 ( )
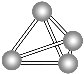
A. N4与N2互为同分异构体
B. N4分子中只含有共价键
C. 1 mol N4分子所含共价键数为4NA
D. N4沸点比P4(白磷)高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个固定容积的密闭容器中,保持一定温度进行如下反应:H2(g)+Br2(g)![]() 2HBr(g),已知加入1 mol H2和2 mol Br2达到平衡后,生成x mol HBr,在相同条件下若起始时加入的H2、Br2、HBr分别为a、b、c(均不为0)且保持平衡时,各组分含量都不变,以下推断正确的是
2HBr(g),已知加入1 mol H2和2 mol Br2达到平衡后,生成x mol HBr,在相同条件下若起始时加入的H2、Br2、HBr分别为a、b、c(均不为0)且保持平衡时,各组分含量都不变,以下推断正确的是
①a、b、c应满足的关系是4a+c=2b
②平衡时HBr为ax mol
③a、b、c应满足的关系是a+b=c
④平衡时HBr为![]() x mol
x mol
A. ① B. ①② C. ①④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)被称为21世纪的新型燃料,以CO和H2为原料生产二甲醚主要发生以下三个反应:
(1)该工艺的总反应为3CO(g)+3H2(g)![]() CH3OCH3(g)+CO2(g) ΔH=_________,化学平衡常数K=______________(用含K1、K2、K3的代数式表示)。
CH3OCH3(g)+CO2(g) ΔH=_________,化学平衡常数K=______________(用含K1、K2、K3的代数式表示)。
化学反应方程式 | 化学平衡常数 | |
①CO(g)+2H2(g) | ΔH1=-99 kJmol-1 | K1 |
②2CH3OH(g) | ΔH2=-24 kJmol-1 | K2 |
③CO(g)+H2O(g) | ΔH3=-41 kJmol-1 | K3 |
(2)某温度下,将8.0molH2和4.0molCO充入容积为2L的密闭容器中,发生反应:4H2(g)+2CO(g) ![]() CH3OCH3(g)+H2O(g),10 分钟后反应达平衡,测得二甲醚的体积分数为25%,则用H2表示的反应速率为_________,CO的转化率为________。
CH3OCH3(g)+H2O(g),10 分钟后反应达平衡,测得二甲醚的体积分数为25%,则用H2表示的反应速率为_________,CO的转化率为________。
(3)下列措施中,能提高CH3OCH3产率的有________。
A.分离出二甲醚 B.降低温度 C.改用高效催化剂D.增大压强
(4)该工艺中反应③的发生提高了CH3OCH3的产率,原因是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.5g NaOH、NaHCO3、Na2CO3固体粉末溶于水,制成溶液,然后逐渐向其中滴加1mol/L的盐酸,所加入盐酸的体积与产生的CO2的体积(标准状况)的关系如图像所示:

(1)写出OA段发生的离子反应方程式___________________、___________________________
(2)当加入35mL盐酸时,产生CO2的体积为_________________(标准状况)
(3)原混合物中NaOH的质量为_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CO(g) + H2O(g) ![]() H2(g) + CO2(g) 的平衡常数K随温度的变化如下表,下列说法正确的是( )
H2(g) + CO2(g) 的平衡常数K随温度的变化如下表,下列说法正确的是( )
温度/℃ | 400 | 500 | 830 | 1000 |
平衡常数K | 10 | 9 | 1 | 0.6 |
A. 该反应的正反应是吸热反应
B. 恒温时增大压强,正反应速率增大
C. 830℃时,反应达到平衡,一定是c(CO)=c(CO2)
D. 400℃时,生成CO2物质的量越多,平衡常数K越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对比类推法是一种常用的学习和研究方法。下列离子方程式的书写正确且类推合理的是
选项 | 离子方程式 | 类推 |
A | 家庭漂白原理:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO | 向漂白粉溶液中通入少量的SO2气体:Ca2++2ClO-+H2O+SO2=CaSO3↓+2HClO |
B | 向FeBr2溶液中通入少量的Cl2:2Fe2++Cl2=2Fe3++2Cl- | 向FeI2溶液中通入少量的Cl2:2Fe2++Cl2=2Fe3++2Cl- |
C | 用石墨电极电解NaCl饱和溶液:2H2O+2Cl- | 用石墨电极电解AlCl3饱和溶液:2H2O+2Cl- |
D | 明矾净水:Al3++3H2O | 硫酸铁净水:Fe3++3H2O |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容积固定为3 L的某密闭容器中加入1 mol A、2 mol B,一定温度下发生如下反应:A(s)+2B(g)![]() C(g)+D(g),经反应5 min后,测得C的浓度为0.3 mol·L-1。则下列说法中正确的是
C(g)+D(g),经反应5 min后,测得C的浓度为0.3 mol·L-1。则下列说法中正确的是
A. 5 min内D的平均反应速率为0.02 mol·L-1·min-1
B. 5 min内A的平均反应速率为0.06 mol·L-1·min-1
C. 经5 min后,向容器内再加入C,正反应速率变小
D. 平衡状态时,生成1 mol D时同时生成1 mol A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com