
| 实验序号 | 操作现象 |
| i | 取少量固体样品,加入过量稀盐酸,固体溶解,产生气体(经检验为H2),溶液呈浅黄色 |
| ii | 向i所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液,产生无色气体(经检验为O2,溶液变为深红色) |
分析 (1)反应中吸热、放热与反应条件没有必然关系,需要根据反应物总能量与生成物总能量大小进行比较;铝热反应中由于铝的还原性较强,所以才能够将还原性弱的金属置换出来;
(2)铝与氧化铁在高温下发生反应生成氧化铝和铁,据此写出反应的化学方程式;
(3)取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色,说明溶液中含有铁离子;向i所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液,产生无色气体(经检验为O2),溶液变为深红色,说明加入双氧水后,溶液中亚铁离子被氧化成铁离子,所以溶液由浅红色变为深红色,则溶液中铁元素存在形式为Fe2+、Fe3+;铁离子能够做催化剂,使双氧水分解生成氧气;可以用氢氧化钠溶液鉴别反应后的固体中是否含有金属铝,据此进行解答.
解答 解:(1)a.该反应需在高温下发生,所以是吸热反应:反应吸热、放热与反应条件没有必然关系,该反应中反应物总能量大于生成物总能量,所以该反应为放热反应,故a错误;
b.铝热反应中,由于铝的还原性较强,所以铝能将相对不活泼的金属从其化合物中置换出来,故b正确;
故答案为:b;
(2)铝与氧化铁发生的铝热反应方程式为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,故答案为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3;
(3)取少量固体样品,加入过量稀盐酸,固体溶解,产生无色气体(经检验为H2),溶液呈浅黄色,说明溶液中含有铁离子;向i所得溶液中加入少量KSCN溶液,溶液呈浅红色,再加入H2O2溶液,产生无色气体(经检验为O2),溶液变为深红色,说明加入双氧水后,溶液中亚铁离子被氧化成铁离子,所以溶液由浅红色变为深红色,则溶液中铁元素存在形式为Fe2+、Fe3+,
①根据分析可知,铁元素在溶液中存在形式为:Fe2+、Fe3+,故答案为:Fe2+、Fe3+;
②铁、氧化铁都不与氢氧化钠溶液反应,而铝能够与氢氧化钠溶液反应,所以可用氢氧化钠溶液检验样品中是否含Al单质,反应的离子方程式为:2OH-+2Al+2H2O=2AlO2-+3H2↑;故答案为:NaOH溶液;2OH-+2Al+2H2O=2AlO2-+3H2↑;
③ii中双氧水在铁离子催化作用下分解生成氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑,故答案为:2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑.
点评 本题考查了铝热反应,题目难度中等,涉及铝热反应原理、化学方程式书写、物质检验与鉴别方法等知识,明确铝热反应原理为解答关键,试题侧重考查学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 煤燃烧时,化学能主要转化为热能 | |
| B. | 白炽灯工作时,电能转化为光能 | |
| C. | 电解水生成氢气和氧气时,化学能转化为电能 | |
| D. | 绿色植物进行光合作用时,太阳能转化为化学能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
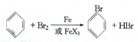
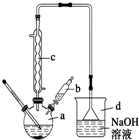 溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:
溴苯是一种常用的化工原料.实验室制备溴苯的实验步骤如下:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 在水中的溶解度 | 微溶 | 微溶 | 微溶 |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于5s | B. | 等于10s | C. | 小于10s | D. | 大于10s |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 变化 | △H | △S | 方向性 | |
| A | H2O(l)→H2O(g) | >0 | <0 | 非自发 |
| B | 2NO2(g)?N2O4(g) | <0 | <0 | 自发 |
| C | 2Fe3+(aq)+Cu(s)=2Fe2+(aq)+Cu2+(aq) | >0 | >0 | 自发 |
| D | NH4Cl(s)=NH3(g)+HCl(g) | <0 | >0 | 非自发 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com