
水是一种重要的资源,节约用水是“全民节约,共同行动”重要的一项。关于水的下列说法
正确的是
A.水可以电离出离子,所以是强电解质
B.水的离子积可表示KW=c(H+)·c(OH-)
C.常温下水中的c(H+)大于c(OH-)
D.升高温度,c(H+)增大,显弱酸性
 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源:2015届江苏省扬州市高二上学期期末考试化学试卷(必修)(解析版) 题型:选择题
下列有关钛原子( )的说法正确的是:
)的说法正确的是:
A.质子数为48 B.中子数为48 C.质量数为22 D.原子序数为22
查看答案和解析>>
科目:高中化学 来源:2015届山东省济宁市高二3月质检化学试卷(解析版) 题型:选择题
下列烃及烃的高聚物:①乙烷;②苯;③聚丙烯;④聚异戊二烯;⑤2-丁炔;⑥环己烷;⑦邻二甲苯;⑧裂解气,能使酸性KMnO4溶液褪色,也能与溴水反应而使溴水褪色的是( )。
A.②③④⑤⑥⑦⑧ B.③④⑤⑥⑦⑧ C.④⑤⑧ D.④⑤⑦
查看答案和解析>>
科目:高中化学 来源:2015届山东省威海市高二上学期期末考试化学试卷(解析版) 题型:选择题
如图为用酸性氢氧燃料电池为电源进行电解的实验装置示意图。下列说法中,正确的是
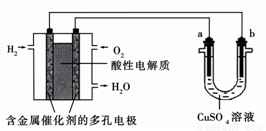
A.燃料电池工作时,正极反应为:O2 + 4H++ 4e-= 2H2O
B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C.a极是含锌、铁的粗铜,b极是纯铜,a极溶解铜的质量与b极析出铜的质量相等
D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等
查看答案和解析>>
科目:高中化学 来源:2015届山东省威海市高二上学期期末考试化学试卷(解析版) 题型:选择题
对于可逆反应:2SO2(g)+O2(g)  2SO3(g) ΔH<0,降低温度产生的影响为
2SO3(g) ΔH<0,降低温度产生的影响为
A. v正 增大,v逆减小 B.v正减小,v逆增大
C. v正和v逆同程度的减小 D. v正和v逆不同等程度的减小
查看答案和解析>>
科目:高中化学 来源:2015届天津市红桥区高二上学期期末考试化学试卷(解析版) 题型:选择题
把0.02 mol/L CH3COOH溶液和0.01 mol/L NaOH溶液以等体积混和后溶液显酸性,则混合液中微粒浓度关系正确的为
A.c(CH3COO-)<c(Na+)
B.c(CH3COOH)+c(CH3COO-)=0.02 mol/L
C.c(CH3COOH)>c(CH3COO-)
D.c(OH-)+c(CH3COO-)=c(H+)+c(Na+)
查看答案和解析>>
科目:高中化学 来源:2015届天津市红桥区高二上学期期末考试化学试卷(解析版) 题型:选择题
某原电池总反应为:Cu+2Fe3+=Cu2++2Fe2+下列能实现该反应的原电池是
ABCD
电极材料Cu、ZnCu、AgCu、CFe、Zn
电解液FeCl3Fe2(SO4)3Fe(NO3)2CuSO4
查看答案和解析>>
科目:高中化学 来源:2015届天津市和平区高二上学期期末考试化学试卷(解析版) 题型:填空题
现有浓度均为0.1mol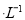 的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题:
的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题:
(l)①、②、③、④四种溶液中由水电离出的浓度由大到小的顺序是___________________
_____________________________________(填序号)。
(2)④、⑤、⑥、⑦四种溶液中NH4+浓度由大到小的顺序是_________________(填序号)。
(3)将③和④按体积比l:2混合后,溶液的pH>7,则混合液中各离子浓度由大到小的顺序是________________________________________。
(4)已知t℃时,Kw=1×10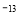 ,则t℃__________(填“>”、“<”或“=”)25℃。在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则 a:b=______________。
,则t℃__________(填“>”、“<”或“=”)25℃。在t℃时将pH=11的NaOH溶液aL与pH=1的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则 a:b=______________。
查看答案和解析>>
科目:高中化学 来源:2015届天津市五区县高二上学期期末考试化学试卷(解析版) 题型:填空题
(1)铁在潮湿的空气中容易发生电化腐蚀最后生成铁锈(Fe2O3.xH2O),则发生腐蚀时正极上发生反应的电极反应式为__________________。
(2)下列哪些装置可防止铁棒被腐蚀__________________。
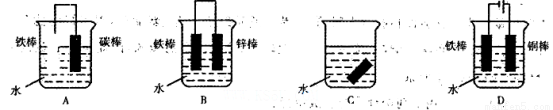
(3)在实际生产中,可在铁件的表面上镀铜防止铁被腐蚀。装置示意图如下左图:

①电镀时,镀件与电源的______________极连接,A电极对应的金属是______________(写元素名称),B电极的电极反应式是______________________。
②上右图是一种钠硫高能电池的结构示意图,M由Na2O和Al2O3制得,其作用是导电和
隔膜,该电池反应为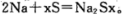 。该电池正极的电极反应式为___________________________。
。该电池正极的电极反应式为___________________________。
用该电池作电源进行上述铁件镀铜时,若电镀池中两电极的质量开始相同,电镀完成后取出洗净、烘干、称量,二者质量差为25.6g,则理论上该电池负极消耗的质量为_________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com