
| A、一部分为Al(OH)3沉淀,一部分以Al3+存在于溶液中 |
| B、一部分为Al(OH)3沉淀,一部分以[Al(OH)4]-形式存在于溶液中 |
| C、全部为Al(OH)3沉淀 |
| D、几乎全部以[Al(OH)4]-形式存在于溶液中 |
科目:高中化学 来源: 题型:
| A、为增加明矾净水效果,可同时加入氢氧化钡溶液 |
| B、计算机硅芯片,光导纤维,普通玻璃都属于硅酸盐产品 |
| C、为防止铁制品生锈,可在铁制品的外层涂油漆或局部镀铜 |
| D、2009年春天为了缓解干旱,许多地方使用AgI或干冰人工降雨过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
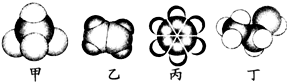
| A、甲能使酸性高锰酸钾溶液褪色 |
| B、乙可与溴水发生取代反应使溴水褪色 |
| C、丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的共价键 |
| D、丁与乙酸都能发生发生中和反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
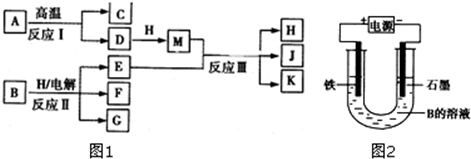
查看答案和解析>>
科目:高中化学 来源: 题型:
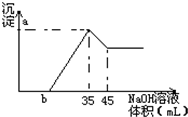 准确称取6g铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有100mLH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/LNaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.试求:
准确称取6g铝土矿(含Al2O3,Fe2O3,SiO2)样品,放入盛有100mLH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/LNaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.试求:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲基橙显黄色的溶液:AlO2-、HCO3-、Na+、K+ |
| B、c(H+)=1×10-1mol?L-1的溶液:IO3-、I-、K+、NH4+ |
| C、各离子物质的量浓度相等的溶液:K+、Na+、SO42-、NO3- |
| D、无色透明的溶液:NH4+、Na+、Cl-、CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 |
| B、日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
| C、用Al(OH)3制胃酸过多 |
| D、电解AlCl3饱和溶液,可制得金属铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
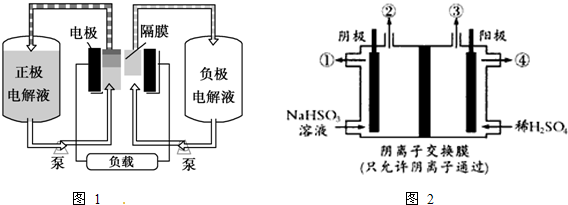
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com