
金属镁可用于制造合金、储氢材料、镁电池等。
已知:①C(s)+O2(g) CO(g) ΔH=-110.5 kJ·mol-1②Mg(g)+O2(g)
CO(g) ΔH=-110.5 kJ·mol-1②Mg(g)+O2(g) MgO(s) ΔH=-732.7 kJ·mol-1
MgO(s) ΔH=-732.7 kJ·mol-1
(1)一种制备镁的反应为MgO(s)+C(s) Mg(g)+CO(g),该反应的ΔH= 。
Mg(g)+CO(g),该反应的ΔH= 。
(2)一种用水氯镁石(主要成分为MgCl2·6H2O)制金属镁工艺的关键流程如下:
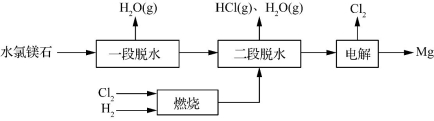
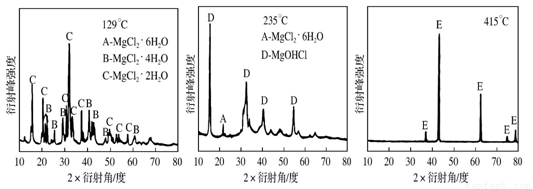
①为探究MgCl2·6H2O“一段脱水”的合理温度范围,某科研小组将MgCl2·6H2O在不同温度下分解,测得残留固体物质的X-射线衍射谱图如下图所示(X-射线衍射可用于判断某晶态物质是否存在)。测得E中Mg元素质量分数为60.0%,则E的化学式为 。 “一段脱水”的目的是制备MgCl2·2H2O,温度不高于180 ℃的原因是 。
②若电解时电解槽中有水分,则生成的MgOHCl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率。生成MgO的化学方程式为 。
(3)Mg2Ni是一种储氢材料。2.14 g Mg2Ni在一定条件下能吸收0.896 L H2(标准状况下)生成X,X的化学式为 。
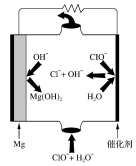
(4)“镁-次氯酸盐”燃料电池的装置如右图所示,该电池反应的电极反应式分别为负极 。 正极
(1)+622.2KJ/mol
(2)MgO 若温度太高,MgCl2转化为MgOHCl或MgO
(3)2MgOHCl+Mg=2MgO+MgCl2+H2↑
(4)Mg2NiH4
(5)Mg-2e-+2OH- =Mg(OH)2↓ ClO-+H2O+2e-= Cl- +2OH-
【解析】
试题分析:(1)根据盖斯定律:①-②得到制备镁的反应为:MgO(s)+C(s)=Mg(g)+CO(g),该反应的△H=+622.2KJ/mol;(2)①分析图谱中温度不同的谱线结合E中镁元素的质量分数为60.0%可知,E为MgO; “一段脱水”的目的是制备MgCl2·2H2O,温度不高于180℃的目的是因为温度过高会生成MgOHCl或MgO;② MgOHCl与Mg反应生成MgO、氯化镁和氢气,化学方程式为:2MgOHCl+Mg=2MgO+MgCl2+H2↑;(3)依据2.14g Mg2Ni在一定条件下能吸收0.896L H2(标准状况下)生成X的定量关系结合反应前后原子守恒分析得到化学式,2.14g Mg2Ni物质的量为0.02mol,吸收的氢气物质的量为0.04mol,Mg2Ni和氢气物质的量之比为1:2,得到X的化学式为Mg2NiH4;(4)根据“镁-次氯酸盐”燃料电池的装置图中微粒变化结合原子守恒、电荷守恒写出电极反应式。该电池反应的电极反应式分别为:负极Mg-2e-+2OH- =Mg(OH)2↓, 正极ClO-+H2O+2e-= Cl- +2OH-。
考点:考查反应热的计算、盖斯定律,物质制备实验的分析判断,原电池原理、化学电源。


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
| A、二氧化氮和二氧化碳 | B、一氧化碳和二氧化碳 | C、二氧化硫和二氧化碳 | D、二氧化硫和二氧化氮 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省湛江市毕业班调研测试理综化学试卷(解析版) 题型:推断题
(16分)某兴趣小组以乙烯等为主要原料合成药物普鲁卡因:
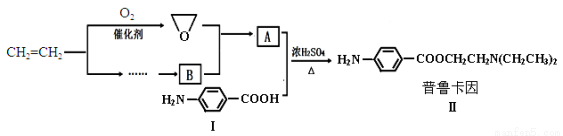
已知: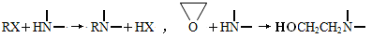
(1)对于普鲁卡因,下列说法正确的是________。
A.一个分子中有11个碳原子 B.不与氢气发生加成反应 C.可发生水解反应
(2)化合物Ⅰ的分子式为 ,1mol化合物Ⅰ能与 mol H2恰好完全反应。
(3)化合物Ⅰ在浓H2SO4和加热的条件下,自身能反应生成高分子聚合物Ⅲ,写出Ⅲ的结构简式_____。
(4)请用化学反应方程式表示以乙烯为原料制备B(无机试剂任选)的有关反应,并指出所属的反应类型___________________________。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高一上学期期中联考化学试卷(解析版) 题型:选择题
同温、同压下,决定气体体积的主要因素是
A、气体分子的直径 B、气体的分子数目
C、气体分子间的平均距离 D、气体分子的摩尔质量
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高一上学期期中联考化学试卷(解析版) 题型:选择题
下列分散系中,分散质微粒半径最小的是
A、雾 B、KCl溶液
C、蛋白质 D、新制Cu(OH)2悬浊液
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
温度为T时,向2.0 L恒容密闭容器中充入2.0 mol NO2,反应2NO2(g) N2O4(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
N2O4(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(N2O4)/mol | 0 | 0.12 | 0.18 | 0.20 | 0.20 |
下列说法正确的是
A.反应在前50 s的平均速率为v(NO2)=0.001 2 mol·L-1·s-1
B.保持温度不变,向平衡后的容器中充入1.0 mol N2O4时,v(正)<v(逆)
C.保持其他条件不变,升高温度达到新平衡时K=0.125,则反应的ΔH<0
D.T温度时,若起始向容器中充入2.0 mol N2O4,则平衡时N2O4的转化率大于80%
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.向氯化铝溶液通入过量的氨气:Al3+ +4OH- AlO2- +2H2O
AlO2- +2H2O
B.过量氯气通人溴化亚铁溶液中2Cl2 +2Fe2+ +2Br- 4Cl-+2Fe3++ Br2
4Cl-+2Fe3++ Br2
C.次氯酸钠与浓盐酸反应产生Cl2:ClO-+Cl—+H2O=Cl2↑+2OH—
D.NaHCO3溶液与少量Ba(OH)2溶液反应:Ba2++2OH-+2HCO3-=BaCO3↓+CO32—+2H2O
查看答案和解析>>
科目:高中化学 来源:2015届江苏省、常州一中、沭阳中学高三联合调研化学试卷(解析版) 题型:选择题
普伐他汀是一种调节血脂的药物,其结构简式如下图所示(未表示出其空间构型)。下列关于普伐他汀的性质描述正确的是

A.能与FeCl3溶液发生显色反应
B.能使酸性KMnO4溶液褪色
C.能发生加成、取代、消去反应
D.1mol该物质最多可与1molNaOH反应
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三质量调研化学试卷(解析版) 题型:选择题
向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如下图所示。有关说法不正确的是

A.线段BC代表Fe3+ 物质的量的变化情况
B.原混合溶液中n(FeBr2)=6mol
C.当通入Cl2 2mol时,溶液中已发生的离子反应可表示为:
2Fe2++2I-+2Cl2=2Fe3++I2+4Cl-
D.原溶液中n(Fe2+): n(I-): n(Br-)=2:1:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com