
��12�֣���ͬŨ�ȵ�������п��Ӧʱ��������Ա���ԭΪSO2��Ҳ�ɱ���ԭΪH2��Ϊ����֤��һ��ʵ��ijͬѧ������ͼ��ʾװ�ý���ʵ�飨ʵ��ʱѹǿΪ101 kPa���¶�Ϊ0 �棩��
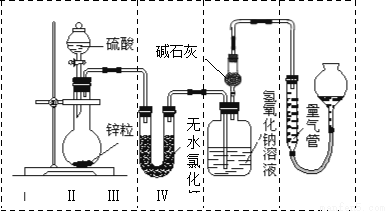
��1��������ƿ�з���0.65 gп������c mol��L��1��H2SO4��Ӧ��Ϊ��֤ʵ����۵Ŀɿ��������ܵ����˹���� ��
A��200 mL B��300 mL C��400 mL
��2����0.65gп����ȫ�ܽ⣬װ�â� ����0.64 g����Բ����ƿ�з�����Ӧ�Ļ�ѧ����ʽΪ
��
��3������ƿ��Ͷ��a gп����ȫ��Ӧ����������ϴ��ƿ����b g�����������ռ���V mL���壬���У�a g��65 g��mol��1��2��b g��64 g��mol��1��2+V mL��22400 mL��mol��1��2���õ�ʽ���ݵ�ԭ���� ��
��4��������ƿ��Ͷ��10gп������һ������18 mol��L��1Ũ����10 mL����ַ�Ӧ��п��ʣ�࣬���װ�â� ����3.2 g��������ʵ����̲����������У�m(SO2)/m(H2)= ��������װ�â���ʢ����ˮ�Ȼ��Ƶ�U�ιܣ�m(SO2) / m(H2)����ֵ�� ���ƫ����ƫС������Ӱ�족����
��1��B ��2��Zn��2H2SO4(Ũ) =ZnSO4��SO2����2H2O
��3��ת�Ƶ����غ� ��4��20��1 ƫ��
��������
�����������1��Ϊ��֤ʵ����۵Ŀɿ���
Zn+H2SO4=ZnSO4+H2��
1mol 22.4L
 0.448L
0.448L
0.448L=448mL����ѡ500mL����Ͳ��
��2�����������Ǽ�������������壬��������ϴ��ƿ����˵���������������ɣ���п�����ᷴӦʱ��п����ԭ����������������������ԭΪ���������ɣ�1�������֪��1.30gп�����ᷴӦ��ֻ���ɶ�����������0.02mol������Ϊ0.02mol��64g/mol=1.28g�����������������Ǻϣ��ʷ�����Ӧ�Ļ�ѧ����ʽΪ��Zn+2H2SO4��Ũ�� ZnSO4+SO2��+2H2O����3������������ԭ��Ӧ�е�ʧ����������г�ʽ�ӣ�����ƿ��Ͷ��a gп����ȫ��Ӧ����������ϴ��ƿ����b g������ƿ���ռ���Vml���壬�����ݻ�ѧ��Ӧ����ʽ��Zn+2H2SO4��Ũ��
ZnSO4+SO2��+2H2O����3������������ԭ��Ӧ�е�ʧ����������г�ʽ�ӣ�����ƿ��Ͷ��a gп����ȫ��Ӧ����������ϴ��ƿ����b g������ƿ���ռ���Vml���壬�����ݻ�ѧ��Ӧ����ʽ��Zn+2H2SO4��Ũ�� ZnSO4+SO2��+2H2O��Zn+H2SO4=ZnSO4+H2�����ɵ����غ���ʽ�����У�
ZnSO4+SO2��+2H2O��Zn+H2SO4=ZnSO4+H2�����ɵ����غ���ʽ�����У� =
=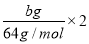 +
+ ���õ�
���õ� ����Ϊ����ʧ�����غ㣻��4��������ƿ��Ͷ��10 gп������һ������18 mol/L Ũ����10mL����ַ�Ӧ��п��ʣ�࣬�����������ϴ��ƿ����3.2g����SO2�����ʵ���Ϊ
����Ϊ����ʧ�����غ㣻��4��������ƿ��Ͷ��10 gп������һ������18 mol/L Ũ����10mL����ַ�Ӧ��п��ʣ�࣬�����������ϴ��ƿ����3.2g����SO2�����ʵ���Ϊ =0.05mol��
=0.05mol��
Zn+2H2SO4��Ũ�� ZnSO4+SO2��+2H2O
ZnSO4+SO2��+2H2O
2mol 1mol
0.1mol 0.05mol
���ɶ���������Ҫ������Ϊ0.1mol��
Zn+H2SO4=ZnSO4+H2��
1mol 1mol
18mol/L��0.01L-0.1mol nmol
��n=0.08mol������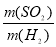 =
= ��������װ�â���ʢ����ˮ�Ȼ��Ƶ�U�ιܣ���III�������������ӵ�����ƫ���������������ƫ������
��������װ�â���ʢ����ˮ�Ȼ��Ƶ�U�ιܣ���III�������������ӵ�����ƫ���������������ƫ������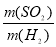 ƫ��
ƫ��
���㣺��������ʵ�鷽������ơ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��4�ֻ����Һ���ֱ��ɵ����0��1 mol��L��2����Һ��϶��ɣ���CH3COONa��HCl����CH3COONa��NaOH����CH3COONa��NaCl����CH3COONa��NaHCO3�����и���������ȷ����
A��pH����>��>��>�� B��c(CH3COOһ)����>��>��>��
C����Һ��c(H+)����>��>��>�� D��c(CH3COOH)�� ��>��>��>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��һ��ѧ�ڵ����ο��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ȥ��Һ��Al3+Ч����õ����ӻ�������
A��Cl- B��OH- C��SO42- D����ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ�ڵ����ο��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йػ�ѧ������ȷ����
����ϩ�����ʽC2H4
���Ҵ��Ľṹ��ʽC2H6O
�����Ȼ�̼�ĵ���ʽ 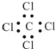
����Ȳ�Ľṹ��ʽCHCH
������ĽṹʽCH3CH3
����ȩ�Ľṹ��ʽCH3COH��
A��ȫ�� B��ȫ�� C���ۢܢ� D���ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ�ڵ����ο��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ȷ����
A����AlCl3��Һ��NaAlO2��Һ�ֱ����ɺ����գ����ù�������ΪAl2O3
B�����ڿ��淴ӦN2(g)+3H2(g) 2NH3(g)������Ũ�ȿ����ӻ���Ӱٷ������Ӷ�ʹ��Ӧ��������
2NH3(g)������Ũ�ȿ����ӻ���Ӱٷ������Ӷ�ʹ��Ӧ��������
C�������£���Mg(OH)2�м��뱥���Ȼ����Һ��ʹMg(OH)2�ܽ�
D�������ܱ������н��еķ�Ӧ3A��g�� B��g��+C��g����������������������£��ٳ���һ������A���壬A��ת���ʽ���С
B��g��+C��g����������������������£��ٳ���һ������A���壬A��ת���ʽ���С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ˮ�и�һ��ѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��8g Na2O2��Na2O��Na2CO3��NaOH�Ĺ��������400g��������Ϊ3.65%������ǡ�÷�Ӧ��������Һ�����յù�������Ϊ
A��16g B��23.4g C��31g D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ˮ�и�һ��ѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���ӷ���ʽH�� + OH��= H2O�ɱ�ʾ�Ļ�ѧ����ʽ��
A��������������ͭ�ķ�Ӧ B�������������������Ƶķ�Ӧ
C��������������þ�ķ�Ӧ D�������백ˮ�ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��ˮ�и߶���ѧ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͼʾ���Ӧ�������������

A��ͼ���ʾ����μӵ�0.1 mol/Lij����Һ�õ��ĵζ����ߣ�����֪Ũ������ζ�δ֪Ũ�ȸü�ʱ���ѡȡ��̪��ָʾ��
B��ͼ���ʾһ�������½��еķ�Ӧ2SO2��O2 2SO3 ���ɷֵ����ʵ����仯��t2ʱ�̸ı��������������С�������
2SO3 ���ɷֵ����ʵ����仯��t2ʱ�̸ı��������������С�������
C��ͼ���ʾij������Һ�м���Ba(OH)2��Һ�����������������Ba(OH)2��Һ����Ĺ�ϵ���ڼ���20 mL Ba(OH)2 ��Һʱ������ǡ�ó�����ȫ
D��ͼ����ʾpH��ͬ������������зֱ����ˮ����ҺpH�ı仯����������a��Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015���ɹŰ������и�һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��16��ʵ����Ҫ����0.1mol/L��ϡ����980mL���ش��������⣺
��1����Ҫ98%�ܶ�Ϊ1.84g/cm3��Ũ���� ______ mL
��2������ʱ������ʹ�õ������� ______ (�����) ��ȱ�ٵ������� ______��______ ��
���ձ� ��10 mL��Ͳ ��20 mL��Ͳ ��������ƽ(������) �ݲ�����
��3������ʱ����ʵ�������õ��������������÷ֱ���______�� ______ ��
��4�����ƹ����г��������������������ҺŨ���к�Ӱ�죨�ƫ�ߡ���ƫ�͡�����Ӱ�족��
������Ͳ��ȡ98%������ʱ���ӡ��� ��
�������ˮ�����˿̶��ߣ�ȡ��ˮʹҺ��ǡ�õ��̶��ߡ��� ��
������ƿû�и���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com