
【题目】Ⅰ.现有下列十种物质:①Cl2 ②钠 ③醋酸(CH3COOH) ④CO2 ⑤H2SO4 ⑥熔融KNO3 ⑦氨水 ⑧稀硝酸 ⑨Al2(SO4)3固体 ⑩NaHCO3,回答下列问题:
(1)属于电解质且能导电是____________(填序号)。
(2)写出①与水反应的化学方程式_____________________________。
(3)写出⑩溶于水时的电离方程式_____________________________。
Ⅱ.按要求回答下列问题:
(1)画 出 Cl-结构示意图 :____________。
(2)请用![]() 的形式,写出质子数为8,中子数为10的微粒符号_______。
的形式,写出质子数为8,中子数为10的微粒符号_______。
(3)某金属氯化物 MCl2 40.5g 中含有 0.6mol Cl-,则M的摩尔质量为____。
(4)相同温度和体积的 A 和 B 两容器,A容器中充满CO2,B容器中充满 O3,若密度相同,则二氧化碳和臭氧的物质的量之比为:_______。
(5)将24.5g H2SO4溶于水配成500mL溶液,其中SO42-的物质的量浓度为__________。
【答案】⑥ Cl2+H2O ![]() HCl+HClO NaHCO3=Na++HCO3-
HCl+HClO NaHCO3=Na++HCO3- 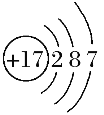
![]() O; 64g/mol 12:11 0.5mol/L
O; 64g/mol 12:11 0.5mol/L
【解析】
Ⅰ.(1)①Cl2、②钠是单质,⑦氨水、⑧稀硝酸是混合物,所以①②⑦⑧既不是电解质也不是非电解质; ④CO2是非电解质;③醋酸(CH3COOH)、⑤H2SO4、⑥熔融KNO3、⑨Al2(SO4)3固体、⑩NaHCO3是电解质,但能导电的只有⑥熔融KNO3,故答案为:⑥;
(2)Cl2与水反应生成盐酸和次氯酸,是可逆反应,方程式为 Cl2+H2O ![]() HCl+HClO ;
HCl+HClO ;
(3)碳酸氢钠为强电解质,全电离,但碳酸是弱酸,碳酸氢根离子不拆,电离方程式为NaHCO3=Na++HCO3- ;
Ⅱ.(1)氯为17号元素,氯离子最外层为8个电子,Cl-结构示意图 :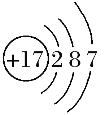 。
。
(2)质子数为8,中子数为10的微粒,质量数为18,符号为![]() O。
O。
(3)某金属氯化物 MCl240.5g中含有 0.6mol Cl-,则n(MCl2)=n(Cl-)/2=0.6mol×1/2=0.3mol,M(MCl2)=40.5g/0.3mol=135g·mol-1,则M的相对原子量为:135-35.5×2=64,M的摩尔质量为64g·mol-1;
(4)相同温度和体积的A和B两容器,A容器中充满CO2,B 容器中充满O3,若密度相同,根据m=ρV可知二氧化碳和臭氧的质量相等,则二氧化碳和臭氧的物质的量之比为m/44:m/48=12:11;
(5)24.5g H2SO4的物质的量为:n(H2SO4)=24.5g/98g·mol-1=0.25mol,H2SO4为强电解质,n(SO42-)=n(H2SO4)=0.25mol,则c(SO42-)=0.25mol/0.5L=0.5mol·L-1。


科目:高中化学 来源: 题型:
【题目】元素的基态原子的核外电子有3种能量状态、5种空间状态,X是其中第一电离能最小的元素;元素Y的M层电子运动状态与X的价电子运动状态相同;元素Z位于第四周期,其基态原子的2价阳离子M层轨道全部排满电子。
(1)X基态原子的电子排布式为___________。
(2)X的氢化物(H2X)在乙醇中的溶解度大于H2Y,其原因是___________。
(3)在Y的氢化物(H2Y分子中,Y原子轨道的杂化类型是___________。
(4)Y与X可形成YX32-。
①YX32-的立体构型为___________(用文字描述)。
②写出一种与YX32-互为等电子体的分子的化学式___________。
(5)Z的氯化物与氨水反应可形成配合物[Z(NH3)4(H2O)2]Cl2,该配合物加热时,首先失去配离子中的配体是___________(写化学式)。

(6)Y与Z所形成化合物晶体的晶胞如图所示,该化合物的化学式为___________。其晶胞边长为540.0pm,密度为___________g·cm-3(列式并计算),a位置Y与b位置Z之间的距离为___________pm(列式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不属于四种基本反应类型,但属于氧化还原反应的是( )
A.Fe+CuSO4=FeSO4+Cu
B.AgNO3+NaCl=AgCl↓+NaNO3
C.Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
D.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质发生变化时,所克服的粒子间相互作用属同种类型的是( )
A. 碘与干冰分别受热变为气体
B. 硝酸铵与硝酸分别受热变为气体
C. 氯化钠与氯化氢分别溶解在水中
D. 晶体钠与冰分别受热熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8等。
(1)某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于________(填“晶体”或“非晶体”)。
(2)基态铜原子有________个未成对电子;Cu2+的电子排布式为____________________;在CuSO4溶液中加入过量氨水,充分反应后加入少量乙醇,析出一种深蓝色晶体,该晶体的化学式为____________________,其所含化学键有____________________,乙醇分子中C原子的杂化轨道类型为________。
(3)铜能与类卤素(SCN)2反应生成Cu(SCN)2,1 mol(SCN)2分子中含有σ键的数目为________。(SCN)2对应的酸有硫氰酸(H—S—C≡N)、异硫氰酸(H—N===C===S)两种。理论上前者沸点低于后者,其原因是______________________________________________________________________________________。

(4)ZnS的晶胞结构如图所示,在ZnS晶胞中,S2-的配位数为_______________。
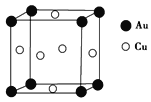
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为________ g·cm-3(用含a、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
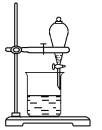
【题目】Ⅰ.某课外活动小组将下图所示装置按一定顺序连接,在实验室里制取一定量的FeCl3(所通气体过量并充分反应)。请回答下列问题:
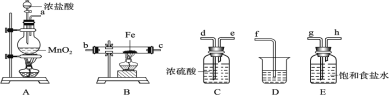
(1)A 中发生反应的化学方程式为________________________。在该反应中当 0.4molHCl发生反应时,生成标准状况下的Cl2 的体积为______。浓盐酸在反应中显示出来的性质是__(填序号);
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)各装置的正确连接顺序为(填写装置代号)A→_____→_____→_____→D。
(3)装置 E 的作用是_______。写出装置 D(D中所盛溶液为 NaOH)中反应的化学方程式_______
(4)工业上用电解法制备氯气的化学方程式为:____________。
Ⅱ.某小组用CCl4萃取碘水中的碘,在下图的分液漏斗中,下层液体呈__________色;他们打开分液漏斗活塞,却未见液体流下,原因可能是__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A+B![]() 3C+4D反应中,表示该反应速率最快的是( )
3C+4D反应中,表示该反应速率最快的是( )
A. υ(A)= 0.5 mol/(L·s) B. υ(B)= 18 mol/(L·min)
C. υ(C)= 0.8 mol/(L·s) D. υ(D)= 1 mol/( L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种工业盐,外观与食盐相似。下面是某学习小组设计的NaNO2制取实验和纯度检验实验。该小组收集了相关资料:
①SO2和HNO3溶液反应生成NOx和H2SO4
②3NO2-+2H+=2NO↑+NO3-+H2O
③NO2-+Ag+=AgNO2↓(AgNO2为淡黄色接近白色固体,在水中形成沉淀)
Ⅰ.亚硝酸钠的制取实验

(1)仪器a的名称为________________________,A装置中发生的化学反应方程式为_____________________________________________。
(2)B装置中多孔球泡的作用是_________________________________________________。
(3)若装置B中逸出的NO与NO2气体物质的量之比为2∶1,则装置B中发生反应的化学方程式为_________________________________________________________。
(4)实验过程中需控制C装置中溶液pH>7,否则C中生成的NaNO2的产量会下降,理由是_____________________________________________________。
(5)请根据题干所给信息设计实验证明C装置中有NO2产生:_________________________________。(限选用的试剂:稀硝酸、硝酸银溶液、NaOH溶液)
Ⅱ.亚硝酸钠的纯度检验
已知:NO2-+MnO4-+H+→NO3-+Mn2++H2O
(6)反应结束后C中溶液通过结晶获得NaNO2粗产品mg,溶解后稀释至250mL,分别取25.00mL用cmol/L的酸性KMnO4溶液平行滴定三次,平均每次消耗酸性KMnO4溶液的体积为VmL。则粗产品中NaNO2的质量分数为_____________(用含c、V、m的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示配制100mL0.100molL﹣1Na2CO3溶液的几个关键实验步骤和操作,据图回答下列问题:
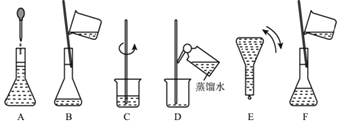
(1)用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是_____。
①干燥的 ②瓶塞不漏水的 ③用欲配制的溶液润洗过的 ④以上三项均须要求的
(2)若用Na2CO310H2O来配制溶液,需要称量晶体_____克。若所称取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度偏_____。(填“大/小”)
(3)写出配制溶液中所需要用到的玻璃仪器的名称:烧杯、_____。
(4)步骤B通常称为转移,步骤A通常称为_____。步骤D称为_____,若没有步骤D,则配制的浓度偏_____。(填“大/小”)。
(5)将上述实验步骤A﹣F按实验过程先后次序排列_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com