
化学反应的本质是旧键断裂和新键形成的过程,下列关于化学反应叙述错误的是( )
A.放热反应△H < 0,吸热反应△H>0
B.化学键断裂释 放能量,化学键形成吸收能量
放能量,化学键形成吸收能量
C.木炭的燃烧是放热反应
D.吸热反应的生成物总能量大于反应物总能量
科目:高中化学 来源:2016-2017学年福建省宁德市高二上期中化学试卷(解析版) 题型:填空题
氨对地球上的生物相当重要,它是许多食物和肥料的重要成分。氨也是制造硝酸、化肥、炸药 的重要原料。氨在国民经济中占有重要地位。回答下列问题:
(1)合成氨工业中,合成塔中每产生2 mol NH3,放出92.2 kJ热量。
①工业合成氨的热化学方程式是_______________。
②若起始时向容器内放入1 mol N2和3 mol H2,达平衡后N2的转化率为20%,则反应放出的热量为Q1 kJ,则Q1的数值为____________;若在同体积的容器中充人2 mol N2和6 molH2,达平衡后放出的热量为Q2 kJ,则Q2__________(填“>”、“<”或“=”)2Q1。
③已知:

1 mol N-H键断裂吸收的能量约等于__________kJ。
(2)在0.5L的密闭容器中,一定量的氮气和氢气进行合成氨反应:N2 (g)+3H2 (g) 2NH3 (g),其平衡常数K与温度T的关系如下表:
2NH3 (g),其平衡常数K与温度T的关系如下表:
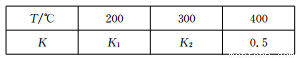
①平衡常数表达式K=_________,K1___________(填“>”、“<”或“一”)K2。
②一定温度下,下列各项能作为判断该反应达到化学平衡状态的依据是__________(填字母)。
a.容器内N2、H2、NH3的浓度之比为1: 3:2
b.浓度商Q=平衡常数K
c.容器内压强保持不变
d.混合气体的密度保持不变
③在400℃时,当测得N2、H2和NH3的物质的量分别为2 mol、1 mol、2 mol时,则此时该反应_________(填“处于”或“不处于”)平衡状态。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省海宁市三校高二下学期期中化学试卷(解析版) 题型:选择题
能够使反应Cu+2H2O=Cu(OH)2+H2↑发生的是
A、铜片作原电池的负极,石墨作原电池的正极,氯化钠作电解质溶液
B、铜锌合金在潮湿空气发生电化学腐蚀
C、用铜片作阴、阳电极,电解硫酸钠溶液
D、用铜片作阴、阳电极,电解硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上学期期中理化学试卷(解析版) 题型:填空题
已知2SO2(g)+O2 (g)
(g) 2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1mol SO3(g)的ΔH= —99kJ/mol。
2SO3(g)反应过程的能量变化如图所示。已知1molSO2(g)氧化为1mol SO3(g)的ΔH= —99kJ/mol。
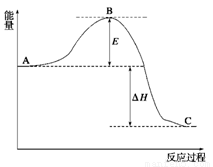
请回答下列问题:
(1) 图中A点表示: ;图中C点表示: ;
图中A点表示: ;图中C点表示: ;
(2)写出 SO3(g)分解成SO2(g)和O2(g)的热化学方程式 ;
(3)能量E在一定条件下可以降低,这种条件是: ;
(4)SO3溶于水可生成H2SO4 ,化学方程式为 ;
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上学期期中理化学试卷(解析版) 题型:选择题
一定温度下,向aL的密闭容器中加入2molNO2(g), 发生如下反应:2NO2  2NO + O2, 此反应达到平衡状态的标志是( )
2NO + O2, 此反应达到平衡状态的标志是( )
A.单位时间内生成2n molNO同时生成2n molNO2
B.单位时间内生成2 n molNO同时生成n molO2
n molNO同时生成n molO2
C.混合气体中NO2、NO和O2的物质的量之比为2﹕2﹕1
D.混合气体中NO2体积分数为50%
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上学期期中理化学试卷(解析版) 题型:选择题
2015年10月10日,中国首届国际山地旅游大会在黔西南州开幕,大会对推动贵州发展生态旅游有着深远的意义。生态旅游的发展需要利用环保的新能源,下列属于新能源的是( )
①天然气 ②太阳能 ③风能 ④石油 ⑤煤 ⑥生物质能 ⑦地热能 ⑧氢能
A.①②③④⑤ B.②③④⑥⑦⑧ C.①②⑤⑥⑦⑧ D.②③⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源:2017届陕西省宝鸡市岐山县高三上期中化学试卷(解析版) 题型:选择题
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是
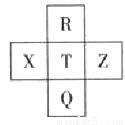
A. 非金属性:Z<T<X
B. R与Q的电子数相差26
C. 气态氢化物稳定性:R <T<Q
D. 最高价氧化物的水化物的酸性: X > T
查看答案和解析>>
科目:高中化学 来源:2017届山西省协作体高三上期中化学试卷(解析版) 题型:填空题
甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成。甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子。A元素原子核内质子数比E的少l,D、E同主族。某同学为探究甲的组成而进行如下实验:
①取mg甲的晶体溶于蒸馏水,配成500 mL溶液;
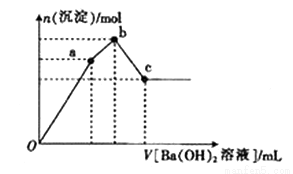
②取少量甲溶液于试管中,逐滴滴入Ba(OH)2溶液,生成沉淀的物质的量与滴入Ba(OH)2溶液体积的关系如图所示;
③取20 mL甲溶液于试管中,加入过量NaOH溶液后加热并收集产生的气体,然后折算成标准状况下的体积为224 mL。
回答下列问题:
(1)D在元素周期表中的位置为_ 。
(2)经测定晶体甲的摩尔质量为453 g·mol-1,其中阳离子和阴离子物质的量之比为1:1。 则晶体甲的化学式为 。
(3)图像中V(Oa):V(ab):V(bc)= 。
(4)写出ab段发生反应的离子方程式: 。
(5)配成的甲溶液物质的量浓度是_ 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省宣城市等四校高二上期中化学卷(解析版) 题型:选择题
在不同温度下,水溶液中c(H+)与c(OH-)有如图所示关系,下列有关说法正确的是( )
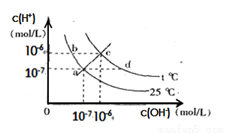
A.c点对应的溶液中大量存在的离子可能为:Na+、H+、Cl-、NO3-
B.将25℃时的KCl溶液加热到t℃,则该溶液中的c(OH-)由a点变化到b点
C.t℃<25℃
D.ac线上的任意一点溶液均有c(H+)=c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com