
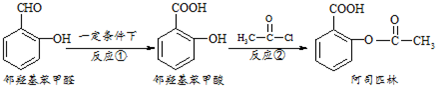
| A. | 与邻羟基苯甲酸互为同分异构体,苯环上一氯代物仅有2种且能发生银镜反应的酚类化合物共有3 种 | |
| B. | 用酸性KMnO4溶液直接氧化邻羟基苯甲醛可实现反应① | |
| C. | 邻羟基苯甲醛不能和溴水发生取代反应 | |
| D. | 1mol阿司匹林最多可以和2molNaOH反应 |
分析 A.与邻羟基苯甲酸互为同分异构体,苯环上一氯代物仅有2种且能发生银镜反应的酚类化合物,含酚-OH及HCOO-结构时,二者位于对位;或含2个酚-OH及1个-CHO,三者相邻且-CHO在中间、或三者位于间位;
B.邻羟基苯甲醛分子中-CHO、酚-OH均能被高锰酸钾氧化;
C.酚羟基邻位、对位含有H原子,可以与溴发生取代反应;
D.阿司匹林含有羧基、酯基,酯基水解得到羧基、酚羟基,而羧基、酚羟基均与氢氧化钠反应.
解答 解:A.与邻羟基苯甲酸互为同分异构体,苯环上一氯代物仅有2种且能发生银镜反应的酚类化合物,含酚-OH及HCOO-结构时,二者位于对位;或含2个酚-OH及1个-CHO,三者相邻且-CHO在中间、或三者位于间位,则符合条件的有3种,故A正确;
B.邻羟基苯甲醛分子中-CHO、酚-OH均能被高锰酸钾氧化,则用酸性KMnO4溶液直接氧化邻羟基苯甲醛不能实现反应①,故B错误;
C.酚羟基邻位、对位含有H原子,可以与溴发生取代反应,故C错误;
D.阿司匹林含有羧基、酯基,酯基水解得到羧基、酚羟基,而羧基、酚羟基均与氢氧化钠反应,1mol阿司匹林最多可以和3molNaOH反应,故D错误.
故选:A.
点评 本题考查有机物的结构和性质、限制条件同分异构体书写,侧重于学生的分析能力的考查,注意把握有机物的官能团的性质,D为易错点,注意阿司匹林中酯基水解得到羧基与酚羟基.


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 分子数和质量分别不等 | B. | 质子数相等,质量不等 | ||
| C. | 分子数和质量都相等 | D. | 原子数、中子数和质子数都相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
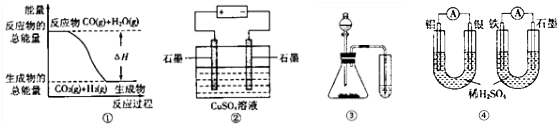
| A. | 图①表示可逆反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H>0 | |
| B. | 图②为电解硫酸铜溶液的装置,一段时间后,阴、阳两极有可能收集到相同体积的气体 | |
| C. | 图③实验装置可完成比较乙酸、碳酸、苯酚酸性强弱的试验 | |
| D. | 图④两个装置中个,通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | |
| B |
| A. | 铍能与冷水发生剧烈反应 | |
| B. | 氢氧化铍既能与强酸溶液反应,又能与强碱溶液反应 | |
| C. | 氢氧化铍的化学式为Be(OH)3 | |
| D. | 氧化铍只溶于强酸溶液,不溶于强碱溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子键就是阴、阳离子间的静电引力 | |
| B. | 所有金属元素与所有非金属元素间都能形成离子键 | |
| C. | NH4Cl属于离子化合物 | |
| D. | 在离子化合物CaCl2中,两个氯离子间也存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | C-H | C=C | C-C | H-H |
| 键能(kJ•mol-1) | 414.4 | 615.3 | 347.4 | 435.5 |
| A. | +288.8kJ/mo1 | B. | -703.4 kJ/mo1 | C. | +125.4kJ/mo1 | D. | -125.4 kJ/mo1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
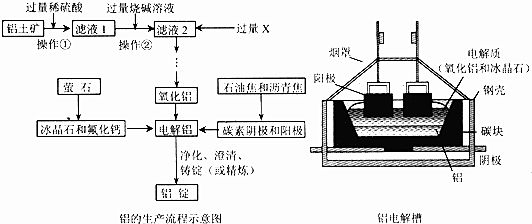
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com