
| A. | ①⑥⑦ | B. | ③⑤⑧ | C. | ③⑦⑧ | D. | ③⑥⑦⑧ |
分析 产生氢气的量不变,则保证铁完全与盐酸反应;加快反应速率,应增大盐酸的浓度或升高温度,据此分析解答.
解答 解:①加水,稀释了盐酸的浓度,故反应速率变慢;
②加硝酸钾溶液相当于加入硝酸,不会生成氢气而生成NO;
③加浓盐酸,氢离子浓度增大,反应速率加快;
④加入铁粉,铁与盐酸反应生成生成氢气的量增多;
⑤加氯化钠溶液,相当于稀释盐酸浓度,氢离子浓度降低,故反应速率变慢;
⑥滴加硫酸铜溶液,铁把铜置换出来,形成原电池,故反应速率加快,但与盐酸反应的铁减少,故减少了产生氢气的量;
⑦升高温度,反应速率加快;
⑧改用浓度大的盐酸,氢离子浓度增大,反应速率加快;
故选C.
点评 本题考查了影响反应速率的因素,为高频考点,侧重考查学生分析判断能力,注意题干中限制性条件“反应速率加快但生成氢气总量不变”,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CH4 | B. | C2H4 | C. | C3H8 | D. | C6H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
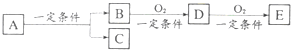 如图,B为常见金属或非金属单质,有下列转化关系.若C是可用作自来水消毒的气体,D、E是氧化物,D转化为E时,增加氧的质量约是D物质总质量的25.8%,则A是( )
如图,B为常见金属或非金属单质,有下列转化关系.若C是可用作自来水消毒的气体,D、E是氧化物,D转化为E时,增加氧的质量约是D物质总质量的25.8%,则A是( )| A. | CuCl2 | B. | AlCl3 | C. | H2O2 | D. | NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
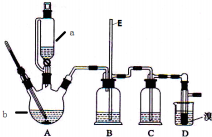 实验室制备1,2一二溴乙烷的反应原理如下:
实验室制备1,2一二溴乙烷的反应原理如下:| 乙醇 | 1.2二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g/cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮是重要的非金属元素,其单质用途之一是制取氨气,反应方程式为:N2(g)+3H2(g)?2NH3(g):回答下列问题:
氮是重要的非金属元素,其单质用途之一是制取氨气,反应方程式为:N2(g)+3H2(g)?2NH3(g):回答下列问题: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
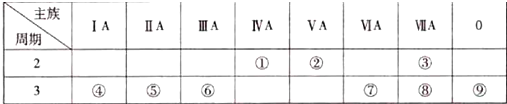
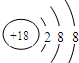 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com