
ij������FeCl2���ʵ�FeCl3��Ʒ����Ҫ�ⶨ������Ԫ�صĺ�����ʵ�鲽�����£�
��ȷ����m g��Ʒ��2~3g����
������Ʒ�м���10mL 5mol/L�����ᣬ�ټ�������ˮ�����Ƴ�250mL��Һ��
����ȡ25mL����������õ���Һ������3mL��ˮ������ʹFe2+��ȫ��������
�ܳ���Ѹ�ټ���Ũ��Ϊ10%�İ�ˮ����������ֽ��裬ʹ֮��ȫ������
�ݹ��ˣ�������ϴ�ӡ����ա���ȴ�������������������ء�
���������������ش�
��1��������ǰ��������ƽ��ָ��ƫ��������������ʱ��ָ��պ��ڱ�ߵ��м䣬��������Ʒ������ ��
A����m g�� B����m g�� C��ǡ��Ϊm g
��2���ܽ���ƷʱҪ�������ᣬԭ���� ��
��3����250mL��Һʱ������250mL����ƿ���ձ��⣬�����õ��IJ��������� �� ��
��4��������ˮʱ������Ӧ�����ӷ���ʽ�� ��
��5������������ΪW1 g�����������պ�������������W2 g������Ʒ����Ԫ�ص����������� ��
��6����������250mL��Һʱ�����õ�����ƿû��ϴ�ɾ�����������������ʱ�����ջ�ʹ��Ԫ�صIJⶨ��������NaCl ����Fe2��SO4��3 ���ƫ�ߡ�����ƫ�͡����䡱����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
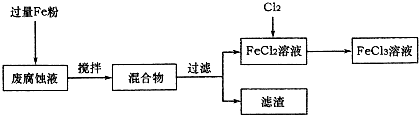
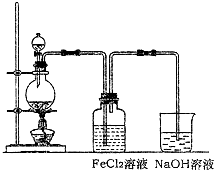
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
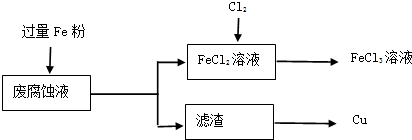
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com