
【题目】硫化氢毒性很大,俗称“一口闷”,工业废水中的硫化物在酸性条件下会以硫化氢的形式逸出。某课外小组以碘量法测定废水中的硫化物,实验装置如图所示,实验步骤及测定原理如下:

Ⅰ.取样、吹气、固硫
连接装置,打开氮气源,检查装置气密性。移取一定体积1mol·L-1乙酸锌溶液于两支吸收管中,取200mL水样于反应瓶中,通入氮气一段时间。移取10mL盐酸于反应瓶中,水浴加热,继续通入氮气。已知乙酸锌与硫化氢反应生成硫化锌沉淀(硫化氢被完全吸收)。
Ⅱ.滴定
关闭气源,往两个吸收管中各加入0.010mol·L-1的碘标准溶液100mL(过量),再加入盐酸5mL,静置。加入淀粉指示液,用0.010mol·L-1的硫代硫酸钠标准溶液对两支吸收管中的液体进行滴定。(已知:![]() )
)
回答下列问题:
(1)水浴加热的温度不能高于85℃,原因是_____________________________。
(2)加入碘标准溶液时,吸收管中发生反应的化学方程式为________________。
(3)该实验使用两个吸收管的原因是_____________________________,若只使用一个吸收管,会导致测定结果偏______________________(填“高”或“低”)。
(4)该200mL水样经吹气、固硫后,滴定操作时共消耗160mLNa2S2O3溶液,则废水中硫的含量为________mg·L-1。
(5)实验室常用FeS固体与酸反应制取H2S。实验室制取H2S时,从反应物与生成物的状态、性质和反应条件分析,下列发生装置中可选用的是________(填序号)。

(6)将二氧化氯溶液加入硫化氢溶液中,然后加入少量稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成。写出二氧化氯与硫化氢溶液反应的离子方程式:____。
【答案】温度太高,硫化氢逸出速率过快,导致不能被完全吸收(或其他合理答案) ZnS+I2=ZnI2+S 保证硫化氢被完全吸收 低 192 bc 5H2S+8ClO2+4H2O=18H++5SO42-+8Cl-
【解析】
硫化氢在反应瓶中制取,开始通入氮气一段时间,排净装置中的空气;水浴加热及充入氮气目的为排净反应瓶中生成硫化氢气体,硫化氢在吸收液中被完全吸收。在吸收管中发生:ZnS+I2=ZnI2+S,剩余的碘单质发生:![]() 。
。
(1)水浴加热温度过高,产生的气体流速过快,导致不能被完全吸收,答案为:温度太高,硫化氢逸出速率过快,导致不能被完全吸收(或其他合理答案);(2)在吸收管中发生:ZnS+I2=ZnI2+S;(3)使用两个吸收管的原因是:产生气体流速过快时,下一个吸收管能够吸收硫化氢气体,保证硫化氢被完全吸收;只使用一个,可能到硫化氢气体不能被完全吸收,结果偏低;(4)0.16L![]() 0.010mol/L:n(I2)=2:1,求得,剩余n(I2)=0.0008mol,共有碘单质:0.1L
0.010mol/L:n(I2)=2:1,求得,剩余n(I2)=0.0008mol,共有碘单质:0.1L![]() 0.010mol/L
0.010mol/L![]() 2=0.002mol,ZnS+I2=ZnI2+S,此反应消耗单质碘:0.0012mol,则n(S2-)=0.0012mol,废水中硫的含量=0.0012mol
2=0.002mol,ZnS+I2=ZnI2+S,此反应消耗单质碘:0.0012mol,则n(S2-)=0.0012mol,废水中硫的含量=0.0012mol![]() 32g/mol/0.2L=192mg/L;(5)FeS固体不溶于水,从节约环保的角度分析可用启普发生器或类似的装置,或可控的反应装置,故答案为:bc;(6)反应中有不溶于酸的白色沉淀生成,则生成BaSO4,根据化合价升降法配平,5H2S+8ClO2+4H2O=18H++5SO42-+8Cl-。
32g/mol/0.2L=192mg/L;(5)FeS固体不溶于水,从节约环保的角度分析可用启普发生器或类似的装置,或可控的反应装置,故答案为:bc;(6)反应中有不溶于酸的白色沉淀生成,则生成BaSO4,根据化合价升降法配平,5H2S+8ClO2+4H2O=18H++5SO42-+8Cl-。


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
【题目】以有机物A(含有苯环的烃,化学式C8H8)和CCl4为原料合成苯丙氨酸E的流程如下:
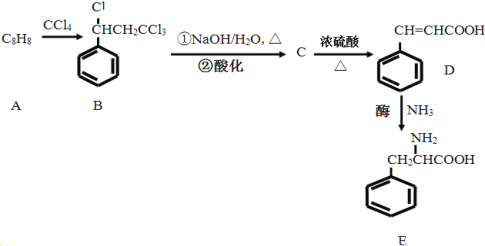
已知:烃分子中的氢原子被卤素原子取代所生成的衍生物叫做卤代烃,如CH3CH2Cl;卤代烃在NaOH水溶液加热条件下会水解,如:
CH3CH2Cl+NaOH![]() CH3CH2OH+NaCl
CH3CH2OH+NaCl
CH2ClCH2Cl+2NaOH![]() CH2OHCH2OH+2NaCl
CH2OHCH2OH+2NaCl
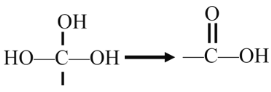 (该反应不需要条件就迅速转化)
(该反应不需要条件就迅速转化)
R-CH2CH2OH![]() R-CH=CH2+H2O
R-CH=CH2+H2O
(1)D→E的反应类型为_____________________。
(2)A的结构简式为________________________。
(3)有关D的叙述错误的是___________(填序号)。
a.能使酸性KMnO4溶液褪色 b.能与溴的CCl4溶液反应
c.能与甲醇发生酯化反应 d.能发生水解反应
(4)C→D反应的化学方程式为___________________________________。
(5)满足下列条件的E的同分异构体共有_________种。
①属于酯类;②苯环上只有两个对位取代基,其中一个为—NH2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入![]() 和
和![]() ,一定条件下使反应
,一定条件下使反应![]() 达到平衡,正反应速率随时间变化的示意图如图所示
达到平衡,正反应速率随时间变化的示意图如图所示![]() 由图得出的结论不正确的是
由图得出的结论不正确的是
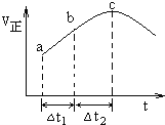
A. 反应过程中压强始终不变
B. 反应物浓度:a点大于b点
C. 反应物的总能量高于生成物的总能量
D. ![]() 时,
时,![]() 的转化率:
的转化率:![]() 段小于
段小于![]() 段
段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是
A. 1molHClO中所含H—Cl键的数目为NA
B. 8.8g乙酸乙酯中所含碳原子数为0.4NA
C. 1.2gC与0.1molCO2在高温下充分反应生成的CO分子数为0.1NA
D. 标准状况下,1L0.1mol·L-1HCl溶液中滴加氨水至pH=7,溶液中NH4+的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知100℃时,水的离子积常数Kw=1×10-12,对于该温度下pH=l1的氨水,下列叙述正确的是
A. 向该溶液中加入同温同体积pH=1的盐酸,反应后溶液呈中性
B. 温度降低至25℃,该氨水溶液中H2O电离出的H+浓度小于10-11mol/L
C. 该氨水溶液中加入NH4Cl溶液,NH3·H2O的电离能力增强
D. 滴加等浓度等体积的硫酸,得到的溶液中存在电离平衡:NH4HSO4(aq)![]() NH4+(aq)+H+(aq)+SO42-(aq)
NH4+(aq)+H+(aq)+SO42-(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语使用正确的是
A. 次氯酸的结构式:H—Cl—O B. 乙醇的结构简式: C2H6O
C. 硫离子的结构示意图:![]() D. 丙烷分子的球棍模型:
D. 丙烷分子的球棍模型:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中,主要不是从安全因素考虑的是
A. 点燃氢气前一定要检验氢气的纯度
B. 未使用完的白磷要随时收集起来,并与空气隔绝
C. 酒精灯不用时,必须盖上灯帽
D. 用氢气还原氧化铜时,要先通一会儿氢气,再加热氧化铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应2SO2+O2![]() 2SO3,反应达平衡的标志是
2SO3,反应达平衡的标志是
①单位时间内消耗2 mol SO2的同时生成2 mol SO3
②反应混合物中,SO2、O2与SO3的物质的量之比为2∶1∶2
③反应混合物中,SO3的质量分数不再改变
A. ①②B. ①③C. ①D. ③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com