
(12分)(1)某一反应体系中有反应物和生成物共5种物质: 、
、 、
、 、
、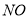 、
、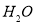 。则该反应中还原产物是______ ;若反应过程中转移了0.3
。则该反应中还原产物是______ ;若反应过程中转移了0.3 电子,则氧化产物的质量_____
电子,则氧化产物的质量_____ 。
。
(2)将a mol Cl2 通入含b mol FeBr2的溶液中,当0< a / b≤1/2 时,反应的离子方程式为:2Fe2+ + Cl2 = 2Fe3+ + 2Cl- ,写出另2个可能发生的离子方程式。
①当 a / b =1时____________________________________________ ;
②当a / b≥3/2时____________________________________________ 。
(3)观察如下反应,总结规律,然后完成下列问题:
①Al(OH)3 +H2O Al(OH)4― + H+ ;②NH3+H2O
Al(OH)4― + H+ ;②NH3+H2O NH4+ + OH―
NH4+ + OH―
(A)已知B(OH)3是一元弱酸,试写出其电离方程式:__________________________;
(B)N2H4是二元弱碱,试写出其第二步电离方程式:_______________________________。
(1)NO 4.8g (2) ①2Cl2 + 2Fe2+ + 2Br― = 4Cl―+ 2Fe3+ + Br2
②3Cl2 + 2Fe2+ + 4Br―= 2Fe3+ + 2Br2 + 6Cl―
(3)B(OH)3+H2O 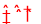 B(OH)4-+H+ N2H5++H2O
B(OH)4-+H+ N2H5++H2O N2H62++OH-
N2H62++OH-
【解析】
试题解析:(1)可根据常见的氧化剂和还原剂来判断HNO3为氧化剂,H2S为还原剂,则NO为还原产物,S为氧化产物。S元素由-2价升高到0价,N元素由+5价降到+2价,应用得失电子守恒规律和观察法配平化学方程式。当生成1mol S时转移2 mol电子,当转移0.3 mol电子生成0.15 mol S,质量为=0.15mol×32g/mol=4.8g;(2)FeBr2的溶液中,还原性Fe2+ >Br― ,所以通入氯气,Fe2+ 先被氯气氧化,反应完后再通氯气,Br― 被氧化。所以当0< a / b≤1/2时,只有Fe2+ 被氧化,所以发生反应2Fe2+ + Cl2 = 2Fe3+ + 2Cl- ;当 a / b =1时,Fe2+ 全部被氧化,Br― 是Fe2+ 的2倍,只有1半被氧化,所以发生的反应方程式为2Cl2 + 2Fe2+ + 2Br― = 2Fe3+ + Br2 + 4Cl― ;当a / b≥3/2时,Fe2+ 、Br―全部被氧化,所以反应为3Cl2 + 2Fe2+ + 4Br― = 2Fe3+ + 2Br2 + 6Cl― ;(3)(A)因为B(OH)3是一元弱酸,所以类似氢氧化铝(偏铝酸)的电离:Al(OH)3 +H2O  Al(OH)4-+ H+ ,所以B(OH)3 应该是与水作用,也生成酸根离子:B(OH)3+H2O
Al(OH)4-+ H+ ,所以B(OH)3 应该是与水作用,也生成酸根离子:B(OH)3+H2O  B(OH)4― + H+ ; (B)N2H4是二元弱碱,则根据②可知,电离方程式为N2H4+H2O
B(OH)4― + H+ ; (B)N2H4是二元弱碱,则根据②可知,电离方程式为N2H4+H2O  N2H5+ +OH-、N2H5+ + H2O
N2H5+ +OH-、N2H5+ + H2O N2H62+ +OH-。
N2H62+ +OH-。
考点:氧化还原反应方程式配平与计算和弱电解质的电离


科目:高中化学 来源:2015届陕西省宝鸡市岐山县高三上学期期中考试化学试卷(解析版) 题型:选择题
将15ml 2mol/LNa2CO3的溶液逐滴加入到40ml 0.5mol/LMCln的盐溶液中,恰好将溶液中的Mn+离子完全沉淀为碳酸盐,则MCln中的n值是
A.3 B.4 C.2 D.1
查看答案和解析>>
科目:高中化学 来源:2015届重庆市高三上期第一次月考理综化学试卷(解析版) 题型:选择题
下述实验不能达到预期实验目的的是
选项 | 实验内容 | 实验目的 |
A | 将2.5 g CuSO4·5H2O溶解在97.5 g 水中 | 配制质量分数为1.6%的CuSO4溶液 |
B | 向盛有1 mL硝酸银溶液的试管中滴加NaCl溶液,至不再有沉淀生成,再向其中滴加Na2S溶液 | 说明一种沉淀能转化为另一种溶解度更小的沉淀 |
C | 取少量待检固体溶于水中,滴加少量Ba(OH)2溶液,观察是否有白色沉淀生成 | 检验NaHCO3固体中是否含Na2CO3 |
D | 取出分液漏斗中所需的上层液体 | 下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体从分液漏斗上口倒出 |
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高二上学期期中考试化学试卷(解析版) 题型:选择题
为了防止热带鱼池中水藻的生长,需保持水中Cu2+的浓度约1.2×10-5 mol·L-1。为避免在每次换池水时溶液浓度的改变,可把适当的含铜化合物放在池底,其饱和溶液提供适当的Cu2+。已知CuS、Cu(OH)2、CuCO3的Ksp值依次为1.3×10-36、2.2×10-20、1.4×10-10,下列四种物质中,能满足池水浓度要求的是
A.CuS B.Cu(NO3)2 C.Cu(OH)2 D.CuCO3
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高二上学期期中考试化学试卷(解析版) 题型:选择题
将0.1mol/L的下列物质的水溶液,从常温加热到80℃(不计水的蒸发),溶液的pH不变的是
A.NaCl B.(NH4)2SO4 C.Ba(OH)2 D.H2SO4
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高一上学期期中考试化学试卷(解析版) 题型:选择题
ClO2是一种广谱型的消毒剂,根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加入H2SO4酸化后反应制得,在该反应中NaClO3和Na2SO3的物质的量之比为
A.3∶1 B.2∶3 C.1∶2 D.2∶1
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高一上学期期中考试化学试卷(解析版) 题型:选择题
2013年10月24日在京沪高速公路扬州境内高邮段发生了一起重大交通事故,是由于大雾引起的汽车追尾。雾属于下列哪种分散系
A.乳浊液 B.溶液 C.胶体 D.悬浊液
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高三上学期10月月考试卷(解析版) 题型:填空题
(7分)现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复):H+、Na+、A13+、Ag+、Ba2+、 OH—、C1—、CO32—、NO3—、SO42—已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。③D溶液与另外四种溶液反应都能产生沉淀。④在E溶液中逐滴加入B溶液,溶液先出现沉淀,当滴加至过量时,沉淀部分溶解。试回答下列问题:
(1)A、C的化学式分别为 、 。
(2)A溶液呈碱性的原因 (用离子方程式表示)。
(3)在100mL0.1mol·L-1的E溶液中,逐滴加入35mL 2mol·L-1NaOH溶液,最终得到沉淀的物质的量为
mol。
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省分校高三上学期期初考试化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是( )
A.氯化铝溶液中加入过量氨水:Al3++4NH3?H2O AlO2-+ 4NH4+ + 2H2O
B.澄清石灰水与少量苏打溶液混合:Ca2+ + OH-+ HCO3- CaCO3↓+ H2O
C.碳酸钙溶于醋酸CaCO3 + 2H+ Ca2++CO2↑+H2O
D.氯化亚铁溶液中通入氯气:2Fe2++ Cl2 2Fe3+ +2Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com