
| A. | 98gH2SO4 | B. | 56gFe | C. | 44.8LHCI | D. | 6gH2 |
分析 通常情况下,物质的量相差不大时,物质所占体积:气体>液态>固体;所以气体体积较大的为C、D;然后根据V=nVm计算出6g氢气的体积,根据计算结果进行比较即可.
解答 解:标准状况下,硫酸为液态,Fe为固态,则98gH2SO4、56gFe所占体积都远远小于44.8LHCl、6gH2的体积;
标准状况下气体摩尔体积约为22.4L/mol,则6g H2在标准状况下的体积为:22.4L/mol×$\frac{6g}{2g/mol}$=67.2L,
则所占体积最大的为6g H2,
故选D.
点评 本题考查了物质的量的计算,题目难度不大,明确常见物质体积与所处状态的关系为解答关键,注意掌握物质的量与气体摩尔体积、摩尔质量等之间的关系,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 除去食盐水中的少量泥沙:过滤,长颈漏斗 | |
| B. | 将水和汽油分离:分液,普通漏斗 | |
| C. | 将碘水中的碘和水分离:萃取,分液漏斗 | |
| D. | 除去自来水中含有的少量Na+和Cl-:蒸发结晶,蒸馏烧瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加HCl的浓度 | B. | 加水 | ||
| C. | 增加同浓度盐酸的体积 | D. | 增加压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
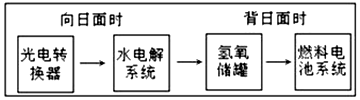 如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是( )
如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH为电解液,下列有关说法中不正确的是( )| A. | 该能量转化系统中的水也是可能循环的 | |
| B. | 燃料电池系统将电能转化为化学能 | |
| C. | 水电解系统中的阳极反应:4OH-═2H2O+O2↑+4e- | |
| D. | 燃料电池放电时的负极反应:H2+2OH-═2H2O+2e- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

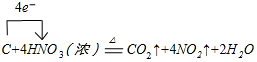 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com