
已知强酸与强碱在稀溶液里反应的中和热可表示为
H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1
对下列反应:
CH3COOH(aq)+NaOH(aq)===CH3COONa(aq)+H2O(l) ΔH=-Q1 kJ·mol-1
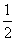 H2SO4(浓)+NaOH(aq)===
H2SO4(浓)+NaOH(aq)===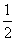 Na2SO4(aq)+H2O(l) ΔH=-Q2 kJ·mol-1
Na2SO4(aq)+H2O(l) ΔH=-Q2 kJ·mol-1
HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l)
ΔH=-Q3 kJ·mol-1
上述反应均在溶液中进行,则下列Q1、Q2、Q3的关系正确的是( )
A.Q2>Q3>Q1 B.Q2>Q1>Q3 C.Q1=Q2=Q3 D.Q2=Q3>Q1
科目:高中化学 来源: 题型:
I.在体积为2L的密闭容器中,加入1mol A与4mol B发生反应:
A(g)+ 2B(g) 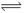 2 C(g) △H= QkJ/mol。达平衡时A的转化率α与温度的变化如下表。
2 C(g) △H= QkJ/mol。达平衡时A的转化率α与温度的变化如下表。
| 温度℃ | 200 | 300 | 500 |
| α | 0.5 | 0.4 | 0.3 |
(1)Q 0(填< 、>、=)。
(2)在200℃时,若经5min达到平衡,则用物质C表示的平均速率为 。
(3)200℃时,将容器体积压缩为1L,平衡时的平衡常数K= 。
II.已知:
由常见的有机物A[CH2=C(CH3)2]可以实现如下的转化:
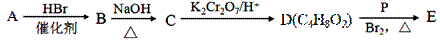
(1)A的系统命名为 ;B→C的反应类型是 。
(2)C的一种同类别的同分异构体M,M能发生催化氧化反应生成醛,则M 的结构简式为 。
(3)写出E与足量的氢氧化钠溶液共热反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C | H—O | C—H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1= kJ·mol-1,已知△H2=-58kJ·mol-1,则△H3= kJ·mol-1。
(2)反应①的化学平衡常数K的表达式为 ;图1中 能正确反映平衡常数K随温度变化关系的曲线为 (填曲线标记字母),其判断理由是 。
能正确反映平衡常数K随温度变化关系的曲线为 (填曲线标记字母),其判断理由是 。

(3)合成气的组成n(H2)/n(CO+CO2)=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而 (填“增大”或“减小”),其原因是 。图2中的压强由大到小为_____,其判断理由是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
有无色溶液,加入Na2O2时有无色无味气体放出,并有白色沉淀生成,加入Na2O2的量与生成白色沉淀的量如图所示.该无色溶液中含有的物质是()
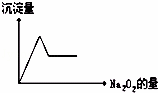
| A. | CaCl2和MgCl2、 | B. | Al2 (SO4)3 | |
| C. | Al2(SO4)3和MgSO4 | D. | Na2SO4和MgSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在1×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是( )
A.H2O(g)===H2(g)+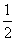 O2(g) ΔH=+242 kJ·mol-1
O2(g) ΔH=+242 kJ·mol-1
B.2H2(g)+O2(g)===2H2O(l) ΔH=-484 kJ·mol-1
C.H2(g)+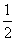 O2(g)===H2O(g) ΔH=+242 kJ·mol-1
O2(g)===H2O(g) ΔH=+242 kJ·mol-1
D.2H2(g)+O2(g)===2H2O(g) ΔH=+484 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
CO(g)+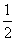 O2(g)===CO2(g) ΔH=-283 kJ·mol-1
O2(g)===CO2(g) ΔH=-283 kJ·mol-1
某H2和CO的混合气体完全燃烧时放出113.76 kJ热量,同时生成3.6 g液态水,则原混合气体中H2和CO的物质的量分别为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
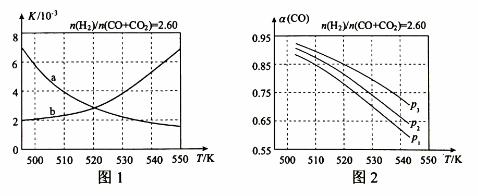
在25°C、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是( )
A.CH3OH(l)+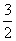 O2(g)===CO2(g)+2H2O(l) ΔH=+725.8 kJ·mol-1
O2(g)===CO2(g)+2H2O(l) ΔH=+725.8 kJ·mol-1
B.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-1 452 kJ·mol-1
C.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=-725.8 kJ·mol-1
D.2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l) ΔH=+1 452 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 | H—H | C—O | C | H—O | C—H |
| E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
由此计算△H1= kJ·mol-1,已知△H2=-58kJ·mol-1,则△H3= kJ·mol-1。
(2)反应①的化学平衡常数K的表达式为 ;图1中能正确反映平衡常数K随温度变化关系的曲线为 (填曲线标记字母),其判断理由是 。
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。α(CO)值随温度升高而 (填“增大”或“减小”),其原因是 。图2中的压强由大到小为_____,其判断理由是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com