
将30mL一定浓度的硝酸与4.51g铜片反应,当铜片全部反应后,共生成2.24L气体(准标状况).则硝酸的物质的量浓度至少为()
A. 9 mol/L B. 8 mol/L C. 5 mol/L D. 10 mol/L
考点: 氧化还原反应的计算.
分析: n(Cu)=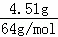 =0.07mol,硝酸与铜反应可能生成NO,NO2、NO的物质的量共为
=0.07mol,硝酸与铜反应可能生成NO,NO2、NO的物质的量共为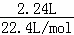 =0.1mol,被还原的硝酸的物质的量等于生成NO2、NO的总的物质的量,硝酸反应后生成硝酸铜、NO和NO2,根据N原子守恒可计算硝酸的物质的量浓度.
=0.1mol,被还原的硝酸的物质的量等于生成NO2、NO的总的物质的量,硝酸反应后生成硝酸铜、NO和NO2,根据N原子守恒可计算硝酸的物质的量浓度.
解答: 解:n(Cu)=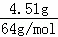 =0.07mol,硝酸与铜反应可能生成NO,NO2、NO的物质的量共为
=0.07mol,硝酸与铜反应可能生成NO,NO2、NO的物质的量共为 =0.1mol,
=0.1mol,
则反应中 消耗HNO3的物质的量为2n+n(NO)+n(NO2)=2×0.07mol+0.1mol=0.24mol,
消耗HNO3的物质的量为2n+n(NO)+n(NO2)=2×0.07mol+0.1mol=0.24mol,
所以原硝酸的物质的量浓度至少为 =8.0mol/L,
=8.0mol/L,
故选B.
点评: 本题考查化学方程式的计算,注意把握硝酸的性质,解答本题的关键是把握氧化还原反应的特点,从质量守恒的角度解答该题,难度不大.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
有一真空瓶质量为m1,该瓶充入空气后质量为m2.在相同状况下,若改为充入某气体A时,总质量为m3.则A的相对分子质量是()
A. 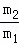 ×29 B.
×29 B.  ×29
×29
C. 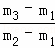 ×29 D.
×29 D.  ×29
×29
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是A、B、C、D、E五种有机物的有关信息;
A B C D E
①能使溴的四氯化碳溶液褪色;②比例模型为:
③能与水在一定条件下反应生成C ①由C、H两种元素组成;
②球棍模型为: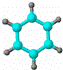 ①由C、H、O三种元素组成;
①由C、H、O三种元素组成;
②能与Na反应,但不能与NaOH溶液反应;
③能与E反应生成相对分子质量为100的酯. ①相对分子质量比C少2;
②能由C氧化而成; ①由C、H、O三种元素组成;
②球棍模型为: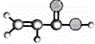
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称叫做 ;写出在一定条件下,A生成高分子化合物的化学反应方程式 .
(2)A与氢气发生加成反应后生成分子F,F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是 (填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与酸性KMnO4溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: .
(4)C与E反应能生成相对分子质量为100的酯,该反应类型为 ;其化学反应方程式为: .
(5)写出由C氧化生成D的化学反应方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语的书写正确的是()
A. 二氧化硅晶体的分子式:SiO2
B. 乙烯的结构简式:CH2CH2
C. F﹣离子结构示意图: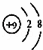
D. 四氯化碳的电子式: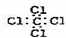
查看答案和解析>>
科目:高中化学 来源: 题型:
从矿物学资料查得,一定条件下自然界存在如下反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4.下列说法正确的是()
A. Cu2S既是氧化产物又是还原产物
B. 5molFeS2发生反应,有10mol电子转移
C. 产物中的SO42﹣离子有一部分是氧化产物
D. FeS2只作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
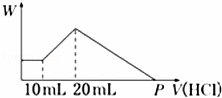
把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中后有0.58 g白色沉淀生成,在所得的浑浊液中,逐滴加入0.5 mol/L盐酸,加入盐酸的体积(V)与生成沉淀的质量(W)关系如图所示:
(1)混合物中NaOH的质量为 g,混合物中AlCl3的质量为 g,混合物中MgCl2的质量为 g.
(2)P点表示盐酸的体积是 mL.
查看答案和解析>>
科目:高中化学 来源: 题型:
配制一定体积、一定物质的量浓度的溶液时,下列操作会使配得的溶液浓度偏小的是( )
|
| A. | 容量瓶中原有少量蒸馏水 |
|
| B. | 溶液从烧杯转移到容量瓶中后没有洗涤烧杯 |
|
| C. | 定容时观察液面俯视 |
|
| D. | 滴管加水时,有少量水滴到容量瓶外 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com