
| A. | 硫 | B. | 氯 | C. | 钠 | D. | 镁 |
分析 元素存在状态由以单质形式存在的为游离态,以化合物形式存在的为化合态,根据元素的活泼性来判断元素在自然界的存在形式,钠、氯、镁性质活泼是以化合态存在,镁主要以化合态存在于海水中,硫以游离态存在.
解答 解:A.硫元素在自然界中火山口附近有游离态的硫元素存在,故A正确;
B.氯是活泼非金属元素,具有强氧化性,易发生反应,自然界中无游离态,故B错误;
C.钠是活泼金属,易失电子自然界中无游离态,故C错误;
D.镁是活泼金属,易失电子自然界中无游离态,故D错误;
故选A.
点评 本题主要考查了元素在自然界的存在形式,注意元素单质的活泼性分析,游离态是单质形式存在,化合态是以化合态存在,题目较简单.


科目:高中化学 来源: 题型:多选题
| A. | SO2+2NaOH═Na2SO3+H2O | B. | SO2+H2O+(NH4)2SO3═2NH4HSO3 | ||
| C. | SO2+N02═SO3+NO | D. | SO2+H2O+Br2═H2SO4+2HBr |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 太阳能蓄电池只是将太阳能直接转化为电能的装置 | |
| B. | 燃料电池是将化学能直接转化为电能的装置,所以能量利用率高 | |
| C. | 碱性Zn-Mn干电池比酸性Zn-Mn干电池耐用,且不易漏液 | |
| D. | 手机上用的锂离子电池属于二次电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O、NH3•H2O、H3PO4 | B. | Cu(OH)2、CH3COOH、C2H5OH | ||
| C. | H2SO3、Ba(OH)2、BaSO4 | D. | H2SiO3、H2S、CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.685mol•L-1 | B. | 3.370 mol•L-1 | C. | 22.49 mol•L-1 | D. | 11.24 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
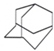 金刚烷的结构如图所示,它可看作是由四个等同的六元环组成的空间构型.判断由氯原子取代金刚烷中的亚甲基(-CH2-)中的氢原子所形成的二氯代物的种类有( )
金刚烷的结构如图所示,它可看作是由四个等同的六元环组成的空间构型.判断由氯原子取代金刚烷中的亚甲基(-CH2-)中的氢原子所形成的二氯代物的种类有( )| A. | 4种 | B. | 3种 | C. | 2种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
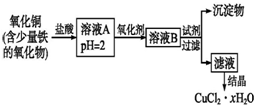 用含少量铁的氧化物的氧化铜制取氯化铜晶体(CuCl2•xH2O).有如下操作:
用含少量铁的氧化物的氧化铜制取氯化铜晶体(CuCl2•xH2O).有如下操作:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com