
选考[选修5:有机化学基础]
充分燃烧1.4 g某有机物A生成4.4 gCO2和1.8 g H2O,该有机物蒸气的密度是相同条件下H2密度的28倍。
(1)该有机物的实验式为________,分子式为________。
(2)A的链状同分异构体共________种。
(3)A的链状同分异构体中含有支链的同分异构体的结构简式为________,其名称为________。
(4)B是A的某种同分异构体,B的磁共振氢谱中只有4个信号峰(即只有4种氢原子),B中官能团为_____(用化学式表示),B通入Br2的CCl4溶液褪色,生成化合物C。则由B生成C的化学方程式为________。
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源:2014-2015安徽省濉溪县高一上学期期末考试化学试卷(解析版) 题型:填空题
(10分)某氧化铝样品中含有氧化铁和二氧化硅杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。请回答下列问题:

(1)沉淀A的成分是 (填化学式),沉淀B的成分是 (填化学式);
(2)写出第④步反应的化学方程式 ;
(3)在操作Ⅰ的名称是 ,其中玻璃棒的作用是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三下学期一模考试化学试卷(解析版) 题型:填空题
(14分)A、B、C、D、E、F均为短周期元素,其原子序数依次增大。已知:A的最外层电子数等于其电子层数;B的最外层电子数是次外层电子数的两倍;D是地壳中含量最高的元素;D和F、A和E分别同主族;E是所有短周期主族元素中原子半径最大的元素。根据以上信息回答下列问题:
(1)B与D形成化合物BD2的结构式为 。
(2)A、C、D三元素能形成一种强酸甲,写出单质B与甲的浓溶液反应的化学反应方程式 。FD2气体通入BaCl2和甲的混合溶液,生成白色沉淀和无色气体CD,有关反应的离子方程式为_____。
(3)均由A、D、E、F四种元素组成的两种盐,其相对分子质量相差16,写出它们在溶液中相互作用的离子方程式为____________________________________;由B、D、E组成的盐溶于水后溶液显碱性,其原因是(用离子方程式表示)_______________。
(4)C2A4─空气燃料电池是一种碱性燃料电池。电解质溶液是20%~30%的KOH溶液。则燃料电池放电时:正极的电极反应式是______________;负极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:选择题
一种微生物燃料电池的结构示意图如下所示,关于该电池的叙述正确的是
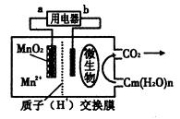
A.电池工作时,电子由a流向b
B.微生物所在电极区放电时发生还原反应
C.放电过程中,H+从正极区移向负极区
D.正极反应式为:MnO2+4H+ +2e— ===Mn2+ +2 H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:选择题
下列化学反应对应的离子方程式书写正确的是
A.醋酸溶液与Mg(OH) 2反应:Mg(OH) 2 +2H+ =Mg2+ +2H2O
B.碳酸钠溶液呈碱性:CO32— +2H2O H2CO3 +2OH—
H2CO3 +2OH—
C.NH4HCO3溶液与过量NaOH溶液反应:NH4+ +OH—=NH3·H2O
D.用惰性电极电解饱和食盐溶液:2Cl—+2H2O 2OH— +Cl2↑+H2↑
2OH— +Cl2↑+H2↑
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邢台市高二上学期期末考试化学试卷(解析版) 题型:填空题
(12分)氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气的燃烧热值高,H2(g) +1/2 O2 (g) = H2O (g) △H = -241.8 kJ·mol-1
化学键 | H-H | O=O | O-H |
键能(kJ·mol-1) | X | 496.4 | 463 |
请根据相关数据计算:H-H的键能X = ________kJ·mol-1。
(2)根据现代工业技术可以用H和CO反应来生产燃料甲醇,其反应方程式如下:
CO2 (g) + H2(g) = H2O + CH3OH(g) △H = -49.00 kJ·mol-1
一定温度下,在体积为1 L的密闭容器中充入1.00 mol CO2和3.00 mol H2,测得CO2和CH3OH的浓度随时间变化如图所示。
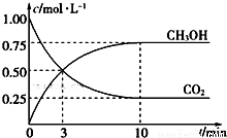
①能说明该反应已达平衡状态的是________(填代号)。
A.CO2在混合气体中的体积分数保持不变
B.单位时间内每消耗1.2 mol H2,同时生成0.4 mol H2O
C.混合气体平均相对分子质量不随时间的变化而变化
D.反应中H2O与CH3OH的物质的量浓度比为1:1,且保持不变
②从反应开始到平衡的平均反应速率v(H2) = ________,达到平衡时氢气的转化率为________。
③该温度下的平衡常数为________(小数点后保留2位)。
④下列的条件一定能加快反应速率并且提高H2转化率的是________(填代号)。
A.升高反应温度
B.缩小容器的体积
C.保持容器体积不变,充入稀有气体
D.保持容器体积不变,充入CO2气体
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邢台市高二上学期期末考试化学试卷(解析版) 题型:选择题
某温度下,H2(g) + CO2(g) = H2O(g) + CO(g)的平衡常数K = 9/4,该温度下在甲、乙、丙三个恒容密闭容器中,投入H2和CO2,其起始浓度如下表所示,下列判断不正确的是
起始浓度 | 甲 | 乙 | 丙 |
c(H2)/mol.L-1 | 0.010 | 0.020 | 0.020 |
c(CO2)/mol.L-1 | 0.010 | 0.010 | 0.020 |
A.平衡时乙中CO2的转化率大于60%
B.平衡时,甲和丙中H2的转化率均是60%
C.平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol/L
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省静宁县高一上学期期末考试化学试卷(解析版) 题型:填空题
(8分)印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”生成CuCl2和FeCl2,其反应的化学方程式:
 Cu + 2FeCl3 ═ CuCl2 + 2FeCl2
Cu + 2FeCl3 ═ CuCl2 + 2FeCl2
(1)请在上式中标出电子转移的方向和数目 。
(2)上述反应中的氧化剂是: 。
(3)写出FeCl3的电离方程式: 。
(4)使用过的腐蚀液会失效,但还可以回收利用,其中有一步需要将Fe2+转化为Fe3+,下列试剂能实现上述变化的是 (填序号)
A.氯气 B.铁 C.双氧水 D.稀硫酸
查看答案和解析>>
科目:高中化学 来源:2014-2015福建省高三上学期期末考化学试卷(解析版) 题型:选择题
关于化学平衡常数K的叙述正确的是
A.K值越大,表示化学反应速率越大
B.对任一可逆反应,温度升高,则K值增大
C.一般情况下K值越大,可逆反应进行得越彻底
D.增大反应物的浓度时,K值增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com