
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是
A.15g 14CO与15N2的混合气体所含质子数为7.5NA
B.11.2L Cl2与NaOH溶液反应,转移电子数为0.5NA
C.2mol SO2与1mol O2反应生成SO3的分子数为2NA
D.6g MgSO4与NaHSO4的混合物所含氧原子数为0.2NA
【答案】D
【解析】
A.14CO与15N2的摩尔质量都是30g·mol 1,并且1个14CO分子与1个15N2分子所含的质子数都是14,所以15 g 14CO与15N2的混合气体的物质的量为![]() =0.5mol,所含的质子数为7NA,A错误;
=0.5mol,所含的质子数为7NA,A错误;
B.未指明标况, 11.2L Cl2的物质的量无法确定,B错误;
C.SO2与 O2在一定条件下反应生成SO3的反应是一个可逆反应,反应物的转化率小于100%,故2mol SO2与1mol O2反应生成SO3的分子数小于2NA,C错误;
D.MgSO4与NaHSO4的摩尔质量都是120g·mol 1,6g MgSO4与NaHSO4的混合物的物质的量为![]() =0.05mol,所含氧原子数为4×0.05mol×NA=0.2NA,D正确;
=0.05mol,所含氧原子数为4×0.05mol×NA=0.2NA,D正确;
答案选D。


 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),H=-akJmol-1,在5L密闭容器投入1molNH3和1mol的O2,2分钟后NO的物质的量增加了0.4mol,下列说法正确的是( )
4NO(g)+6H2O(g),H=-akJmol-1,在5L密闭容器投入1molNH3和1mol的O2,2分钟后NO的物质的量增加了0.4mol,下列说法正确的是( )
A.2分钟反应放出的热量值小于0.1akJ
B.用氧气表示0~2min的反应速率:v(O2)=0.05mol·L-1·min-1
C.2分钟内NH3的转化率是50%
D.2分钟末c(H2O)=0.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证卤素单质氧化性的相对强弱,某学习小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验).

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a.
Ⅳ.
(1)A中产生黄绿色气体,其电子式是 ______;A中使用KMnO4可以在不加热的情况下与浓盐酸发生反应。如果改用二氧化锰,则在加热条件下发生的化学反应方程式为______。
(2)验证氯气的氧化性强于碘的实验现象是 ______ 。
(3)B中溶液发生反应的离子方程式是 ______ 。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 ______。
(5)过程Ⅲ实验的目的是 ______ 。
(6)实验结论:氯、溴、碘单质的氧化性逐渐 ______ ,原因是:同主族元素从上到下 ______ ,得电子能力逐渐 ______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向1L恒容密闭容器中通入2mol CO2和8mol H2发生反应:CO2(g) +4H2(g)![]() CH4(g) +2H2O(g) ,5min后,测得CO2的物质的量为1.2mol ,则0~5min内用H2表示的化学反应速率是
CH4(g) +2H2O(g) ,5min后,测得CO2的物质的量为1.2mol ,则0~5min内用H2表示的化学反应速率是
A.0.16mol·L-1·min -1B.0.24mol·L-1·min -1C.0.64mol·L-1·min -1D.0.96mol·L-1·min -1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表是打开物质世界奧秘之门的一把金钥匙 ,1869年,门捷列夫发现了元素周期律并发表了元素周期表。下图为元素周期表的一部分,回答下列问题。

(1).上述元素中化学性质最稳定的是________(填元素符号,下同) ,非金属性最强的是_____。
(2)c的最高价氧化物对应水化物的化学式为__________。
(3)h元素的原子结构示意图为__________,写出h单质的一种用途:__________。
(4)b、d、f三种元素原子半径由大到小的顺序是__________(用元素符号表示)。
(5)a、g、j的氢氧化物中碱性最强的是__________(填化学式),写出其溶液与g的氧化物反应的离子方程式:___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铝主要用作造纸工业中的沉淀剂和饮用水的絮凝剂。用铝灰(Al2O3、SiO2和少量铁的氧化物)制备硫酸铝晶体[Al2(SO4)3·18H2O]的工艺流程如图所示:
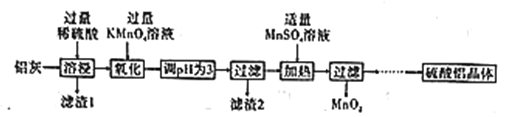
(1)滤渣1的化学式为____。
(2)“氧化”步骤的离子方程式为____。
(3)已知:相关离子生成氢氧化物沉淀的pH范围如表:
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 3.4 | 6.3 | 1.5 |
完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释调节pH为3的目的是________。
(4)“加热”步骤中反应的生成物中氧化产物与还原产物的物质的量之比为_____。
(5)“…”中一系列操作是___、冷却结晶、过滤、___、干燥。
(6)硫酸铝晶体加热发生分解的失重曲线如图所示,主要分为三个阶段:第一阶段失重40.54%,第二阶段失重48.65%,第三阶段失重84.68%,以后不再失重。
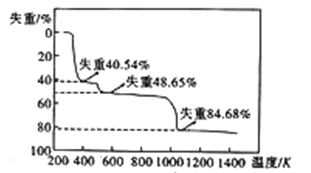
①失重第一阶段残留固体的化学式为_________。
②失重第三阶段反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取 1LFeCl3 溶液腐蚀铜板制作电路板,反应后在此残留液中慢慢加入铁粉,溶液中 Fe2+的浓度变化如图所示(加入固体引起的体积变化忽略不计),下列说法不正确的是

A. 当n(Fe)=0.5mol 时,发生的离子反应为 Fe+2Fe3+=3Fe2+
B. 当 n(Fe)=1.5mol 时,溶液中发生的总反应离子方程式为4Fe3++Cu2++3Fe=7Fe2++Cu
C. 当n(Fe)=1mol 时,溶液中 c(Fe2+)=5 mol·L-1
D. 腐蚀之前原溶液中 c(Fe3+)=4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】脂环烃分子中两个或两个以上碳环共有两个以上碳原子的烃称为桥环烃,二环[4.1.0]庚烷(![]() )是一种典型的桥环烃,下列关于二环[4.1.0]庚烷的说法错误的是( )
)是一种典型的桥环烃,下列关于二环[4.1.0]庚烷的说法错误的是( )
A. 与环庚烯互为同分异构体
B. 所有的碳原子均在同一平面上
C. 一氯代物有4种(不考虑立体异构)
D. 1mol二环[4.1.0]庚烷完全燃烧时消耗10molO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com