
| A. | CO2的结构式:O=C=O | B. | 乙醇分子的球棍模型: | ||
| C. | Cl-结构示意图: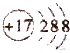 | D. | 四氯化碳的电子式: |
分析 A.二氧化碳为直线型结构,分子中含有两个碳氧双键;
B.乙醇分子中含有1个甲基、1个亚甲基和1个羟基,原子半径C>O>H;
C.氯离子的核电荷数为17,核外电子总数为18,最外层满足8电子稳定结构;
D.四氯化碳分子中,Cl原子最外层满足8电子稳定结构,该电子式中漏掉了Cl原子的3对未成键电子对.
解答 解:A.二氧化碳为共价化合物,分子中含有两个碳氧双键,CO2的结构式为:O=C=O,故A正确;
B.乙醇分子中含有1个羟基,碳原子的原子半径较大,H原子半径最小,乙醇的球棍模型为: ,故B正确;
,故B正确;
C.氯离子的最外层达到8电子稳定结构,其离子结构示意图为: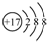 ,故C正确;
,故C正确;
D.四氯化碳分子中含有4个碳氯键,碳原子和氯原子最外层达到8电子稳定结构,四氯化碳正确的电子式为 ,故D错误;
,故D错误;
故选D.
点评 本题考查了常见化学用语的表示方法判断,题目难度不大,涉及电子式、球棍模型、离子结构示意图、结构式等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


科目:高中化学 来源: 题型:选择题
| A. | 向NaAlO2溶液中通入足量的CO2:2AlO${\;}_{2}^{-}$+CO2+3H2O=2Al(OH)3↓+CO${\;}_{3}^{2-}$ | |
| B. | (NH4)2Fe(SO4)2溶液中加入少量氢氧化钡溶液:NH${\;}_{4}^{+}$+SO${\;}_{4}^{2-}$+Ba2++OH-=BaSO4↓+NH3•H2O | |
| C. | NH4Cl浓溶液中滴加浓NaOH溶液并加热:NH${\;}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO${\;}_{3}^{-}$=3Fe3++NO↑+2H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
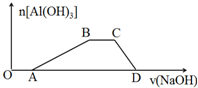 (1)写出工业上分别以①CH2=CH2为原料和②C6H12O6为原料制取乙醇的化学方程式:①CH2=CH2+H2O$→_{高温高压}^{催化剂}$CH3CH2OH②C6H12O6$\stackrel{催化剂}{→}$2CO2↑+2CH3CH2OH
(1)写出工业上分别以①CH2=CH2为原料和②C6H12O6为原料制取乙醇的化学方程式:①CH2=CH2+H2O$→_{高温高压}^{催化剂}$CH3CH2OH②C6H12O6$\stackrel{催化剂}{→}$2CO2↑+2CH3CH2OH查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在氧化还原反应中,还原剂一定是失去电子的反应物 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| C. | 某元素从化合态转变为游离态时,该元素一定被还原 | |
| D. | 金属阳离子被还原不一定得到金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com