
| A、常温下,在空气中金属镁比铁容易氧化 |
| B、在氧气中灼烧时,铁丝比铜丝反应剧烈 |
| C、与同种盐酸反应时,锌片比铁片反应剧烈 |
| D、铜活动性不强,故铜不能与硝酸银溶液反应得到银 |


科目:高中化学 来源: 题型:
| A、NaNO2发生氧化反应 |
| B、NH4Cl中的氮元素被还原 |
| C、N2既是氧化产物,又是还原产物 |
| D、每生成1mol N2转移电子的物质的量为6mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
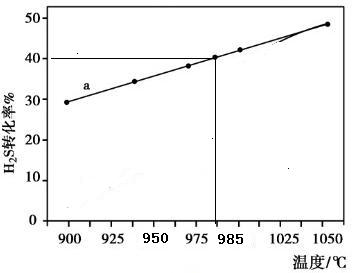
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④ | B、①④ | C、①③ | D、①② |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下,向20mL 0.2mol?L-1 H2A溶液中滴加0.2mol?L-1NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2- ).根据图示判断,下列说法正确的是
常温下,向20mL 0.2mol?L-1 H2A溶液中滴加0.2mol?L-1NaOH溶液.有关微粒的物质的量变化如图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2- ).根据图示判断,下列说法正确的是| A、当V(NaOH)=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| B、等体积等浓度的NaOH溶液与H2A溶液混合后其溶液中水的电离程度比纯水大 |
| C、A点溶液显中性 |
| D、向NaHA溶液加入水的过程中,pH可能增大也可能减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
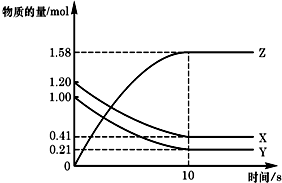 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( )| A、应开始到10 s时,Y的转化率为79.0% |
| B、应的化学方程式为:X(g)+Y(g)=Z(g) |
| C、应开始到10 s,用Z表示的反应速率为0.158mol/(L?s) |
| D、开始到10 s,X的物质的量浓度减少了0.79mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生成了一种强酸弱碱盐 |
| B、强酸溶液和弱碱溶液反应 |
| C、弱酸溶液和强碱溶液反应 |
| D、一元强酸溶液和一元强碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com