
| m |
| n |
| m |
| n |
| 3mol×2g/mol+7mol×32g/mol |
| (3+7)mol |


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
| A、溶液仍为紫色 |
| B、最终溶液褪色,而无其它现象 |
| C、溶液最终变蓝色 |
| D、溶液中有气泡产生,溶液最终变为无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Cl-、Na+、CO32- |
| B、Na+、Ag+、Cl-、NO3- |
| C、Cu2+、Mg2+、SO42-、Cl- |
| D、H+、Na+、Cl-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H<0的反应均是自发反应 |
| B、自发进行的反应一定能迅速进行 |
| C、冰在室温下自动熔化成水,这是熵增的过程 |
| D、高锰酸钾受热分解是一个熵减小的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生铁比纯铁容易生锈 |
| B、钢铁的腐蚀生成疏松氧化膜,不能保护内层金属 |
| C、钢铁发生吸氧腐蚀时,正极反应式为:O2+2H2O+4e-═4OH- |
| D、为保护地下钢管不受腐蚀,可使其与直流电源正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 充电 |
| 放电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
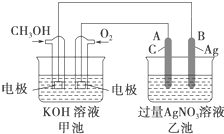 如图是一个化学过程的示意图.已知甲池的总反应式为2CH3OH+3O2+4KOH═2K2CO3+6H2O
如图是一个化学过程的示意图.已知甲池的总反应式为2CH3OH+3O2+4KOH═2K2CO3+6H2O查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com