
| A. | 84消毒液具有碱性,可用作消毒剂和漂白剂 | |
| B. | 氢氟酸具有酸性,可用于玻璃的腐蚀剂 | |
| C. | 过氧化钠具有漂白性,可作航空和潜水的供氧剂 | |
| D. | 活性铁粉具有还原性,在食品袋中可用作除氧剂 |
分析 A.84消毒液用作消毒剂和漂白剂与其强氧化性有关;
B.二氧化硅与HF反应的性质与酸性无关;
C.过氧化钠可与水、二氧化碳反应生成氧气;
D.活性铁粉易与氧气反应.
解答 解:A.84消毒液具有强氧化性,可用作消毒剂和漂白剂,与碱性无关,故A错误;
B.二氧化硅与HF反应的性质与酸性无关,HF与二氧化硅反应生成四氟化硅和水,没有生成盐,HF不表现酸性,故B错误;
C.过氧化钠可与水、二氧化碳反应生成氧气,用作供氧剂与漂白性无关,故C错误;
D.活性铁粉易与氧气反应,消耗氧气,可防止食品变质,故D正确.
故选D.
点评 本题考查较为综合,多角度考查元素化合物知识,侧重于化学与生活的考查,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤⑦ | B. | ③④⑤⑥ | C. | ②④⑤⑦ | D. | ①②④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
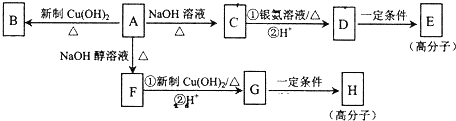
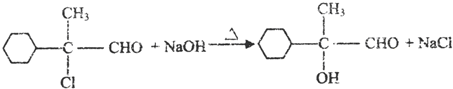 .
.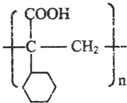 ,E的结构简式是
,E的结构简式是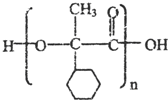 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.0g甲醛和甲酸甲酯的混合物中含有的原子数为0.4NA | |
| B. | 常温下,1L0.1mol•L-1CuSO4溶液中粒子总数小于0.2NA | |
| C. | 1 mol冰醋酸和1 mol乙醇在浓硫酸加热下充分反应生成H2O个数为NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
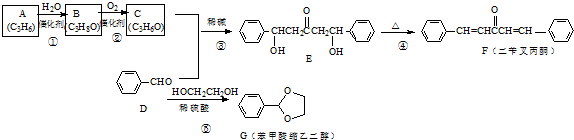
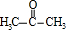 ;A加聚产物的结构简式是
;A加聚产物的结构简式是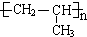 .
.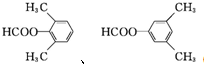 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “地沟油”是指从泔水中提取的油脂,它也是一种资源,但不能食用,可用于生产燃料油或用于制肥皂 | |
| B. | 媒体曝光的制造问题胶囊的工业明胶的主要成分是蛋白质 | |
| C. | 塑化剂DEHP是邻苯二甲酸(2─乙基己基)二酯,对人体无害可用作食品添加剂 | |
| D. | PM2.5是指大气中直径≤2.5×10-6m的颗粒物(气溶胶),可通过加水吸收后再用半透膜渗析的方法分离PM2.5微粒与可溶性吸附物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4,H2O2,NH3 | B. | H2O,CO2,Na2O2 | C. | Na2O,NaCl,MgCl2 | D. | NaOH,NaClO,Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
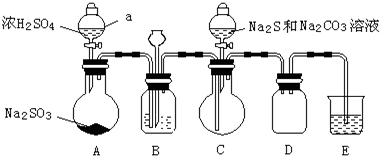
| 推测 | 操作和现象 | 结论 |
| 杂质中的正盐成分可能有: Na2S、Na2CO3 Na2SO4 及 Na2SO3 | ①取Wg产品配成稀溶液; ②向溶液中滴加过量BaCl2溶液,有白色沉淀生成,过滤,得沉淀和滤液; ③向沉淀中加入过量盐酸,沉淀完全溶解,并有刺激性气味的气体产生. | 产品杂质中: 一定含有Na2SO3, 可能含有Na2CO3, 一定不含有Na2S、Na2SO4. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com