
ŅŃÖŖĮņĖį”¢°±Ė®µÄĆܶČÓėĖł¼ÓĖ®ĮæµÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ĻÖÓŠĮņĖįÓė°±Ė®ø÷Ņ»·Ż£¬Ēėøł¾Ż±ķÖŠµÄŠÅĻ¢£¬»Ų“šĻĀĮŠĪŹĢā £ŗ
ČÜÖŹµÄĪļÖŹµÄĮæÅضČ/ | ČÜŅŗµÄĆܶČ/ |
| |
ĮņĖį |
|
| |
°±Ė® |
|
|
£Ø1£©±ķÖŠĮņĖįµÄÖŹĮæ·ÖŹżĪŖ__________(²»Š“µ„Ī»£¬ÓĆŗ¬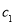 ”¢
”¢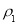 µÄ“śŹżŹ½±ķŹ¾)”£
µÄ“śŹżŹ½±ķŹ¾)”£
£Ø2£©ĪļÖŹµÄĮæÅضČĪŖ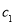
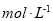 µÄĮņĖįÓėĖ®µČĢå»ż»ģŗĻ(»ģŗĻŗóČÜŅŗĢå»ż±ä»ÆŗöĀŌ²»¼Ę)£¬ĖłµĆČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ___________
µÄĮņĖįÓėĖ®µČĢå»ż»ģŗĻ(»ģŗĻŗóČÜŅŗĢå»ż±ä»ÆŗöĀŌ²»¼Ę)£¬ĖłµĆČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ___________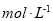 ”£
ӣ
£Ø3£©ĪļÖŹµÄĮæÅضČĪŖ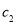
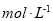 µÄ°±Ė®Óė
µÄ°±Ė®Óė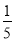
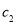
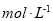 µÄ°±Ė®µČÖŹĮæ»ģŗĻ£¬ĖłµĆČÜŅŗµÄĆܶČ______(Ģī
µÄ°±Ė®µČÖŹĮæ»ģŗĻ£¬ĖłµĆČÜŅŗµÄĆܶČ______(Ģī
”°“óÓŚ”±”¢”°Š”ÓŚ”±»ņ”°µČÓŚ”±£¬ĻĀĶ¬) 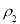
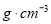 £¬ĖłµĆČÜŅŗµÄĪļÖŹµÄĮæÅضČ________
£¬ĖłµĆČÜŅŗµÄĪļÖŹµÄĮæÅضČ________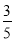
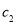
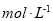
(Éč»ģŗĻŗóČÜŅŗµÄĢå»ż±ä»ÆŗöĀŌ²»¼Ę)
£Ø4£©Čō½«Ļ”ĮņĖįÓė°±Ė®»ģŗĻ£¬Š“³öĘä·“Ó¦µÄĄė×Ó·½³ĢŹ½___________________________.

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢Al3+”¢Cl-”¢CO32- | B£® | Na+”¢Fe3+”¢Cl-”¢NO3- | ||
| C£® | H+”¢Na+”¢ClO-”¢S2- | D£® | K+”¢NH4+”¢OH-”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ŌŖĖŲ | ĢŲÕ÷ |
| X | ÖÜĘŚ±ķÖŠ£¬Ō×Ó°ė¾¶×īŠ” |
| Y | ³£ĪĀĻĀ£¬æÉŅŌŠĪ³ÉY2”¢Y3ŠĶµÄĘųĢåµ„ÖŹ |
| Z | ĘäŌ×ÓÄŚ²ćµē×ÓÓė×īĶā²ćµē×ÓŹżÖ®±ČĪŖ10£ŗ1 |
| W | ×īøß»ÆŗĻ¼ŪĪŖ+6 |
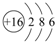 £®
£®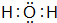 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °±Ė®ÓėŃĪĖįĒ”ŗĆÖŠŗĶŗóµÄČÜŅŗ£ŗc£ØH+£©£¾c£ØOH-£© | |
| B£® | 0.2mol/L“×ĖįČÜŅŗÓė0.1mol/L NaOHČÜŅŗµČĢå»ż»ģŗĻŗóµÄČÜŅŗ£ŗc£ØCH3COO-£©+c£ØCH3COOH£©=0.2mol/L | |
| C£® | NaHSO3ČÜŅŗ£Ø³ŹĖįŠŌ£©£ŗc£ØNa+£©£¾c£ØHSO3-£©£¾c£ØH+£©£¾c£ØOH-£© | |
| D£® | NaHSO4ČÜŅŗµĪČė°±Ė®ŗóµÄČÜŅŗ£ŗc£ØH+£©+c£ØNH4+£©=2c£ØSO42-£©+c£ØOH-£©£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ½Ī÷Ź”øßŅ»ÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®NaCl¹ĢĢåæɵ¼µē
B£®NaHSO4ČÜÓŚĖ®µēĄė³öH+£¬ŌņNaHSO4ŹōÓŚĖį
C£®HClČÜÓŚĖ®Äܵ¼µē£¬µ« ŅŗĢ¬HCl²»Äܵ¼µē
ŅŗĢ¬HCl²»Äܵ¼µē
D£®µ¼µēÄÜĮ¦ĒæµÄČÜŅŗĄļÄܹ»×ŌÓÉŅĘ¶ÆµÄĄė×ÓŹżÄæŅ»¶Ø±Čµ¼µēÄÜĮ¦ČõµÄČÜŅŗĄļÄܹ»×ŌÓÉŅĘ¶ÆµÄĄė×ÓŹżÄæ¶ą
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ½Ī÷Ź”øßŅ»ÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Éč°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµĪŖNA£¬±ź×¼×“æöĻĀO2ŗĶN2µÄ»ģŗĻĘųĢå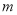 gŗ¬ÓŠbøö·Ö×Ó£¬Ōņ
gŗ¬ÓŠbøö·Ö×Ó£¬Ōņ gøĆ»ģŗĻĘųĢåŌŚĻąĶ¬×“æöĻĀĖłÕ¼µÄĢå»ż(L)Ó¦ŹĒ
gøĆ»ģŗĻĘųĢåŌŚĻąĶ¬×“æöĻĀĖłÕ¼µÄĢå»ż(L)Ó¦ŹĒ
A£®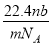 B£®
B£® C£®
C£®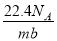 D£®
D£®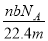
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ°²»ÕŹ”øßŅ»ÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ngO3ŗĶO2µÄ»ģŗĻĘųĢåÖŠŗ¬ÓŠmøöOŌ×Ó£¬Ōņ°¢·üŁ¤µĀĀŽ³£ŹżNAµÄŹżÖµæɱķŹ¾ĪŖ
A£®32m/n B£®16m/n C£®n/32m D£®ĪŽ·Ø¼ĘĖć
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ½ĖÕŹ”øßČżÉĻµŚŅ»“Ī²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃé²Ł×÷Äܹ»“ļµ½ŹµŃéÄæµÄµÄŹĒ
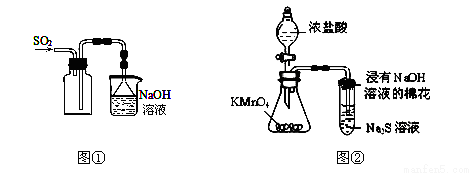
A. ŹµŃéŹŅ²ÉÓĆĶ¼¢ŁĖłŹ¾×°ÖĆŹÕ¼ÆSO2
B. æÉÓĆĶ¼¢ŚĖłŹ¾×°ÖĆ±Č½ĻKMnO4”¢Cl2”¢SµÄŃõ»ÆŠŌĒæČõ
C. ³żČ„NaHCO3ČÜŅŗÖŠµÄNa2CO3£¬æɼÓČėCa(OH)2ČÜŅŗŗó¹żĀĖ
D. ³ĘČ”0.40 g NaOH£¬ÖĆÓŚ100 mLČŻĮæĘæÖŠ£¬¼ÓĖ®Čܽā£¬ÅäÖĘ0.10 mol/L NaOHČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com