
下列事实与氢键有关的是( )
A.水加热到很高的温度都难以分解
B.水结成冰体积膨胀,密度变小
C.CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高
D.HF、HCl、HBr、HI的热稳定性依次减弱
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
MgSO4·7H2O是一种重要的化工原料。某研究性学习小组设计了利用菱镁矿石(主要成分是MgCO3,并含有MnCO3、SiO2杂质)制取MgSO4·7H2O的实验,流程如下。


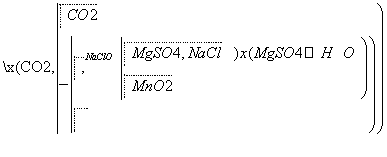
(1)第①步研磨的目的是____________________,所得滤液主要含__________________、__________________等溶质。
(2)第②步反应的离子方程式为_________________________________。
(3)第③步浓缩结晶后,要经过________、洗涤、干燥等步骤才可得到MgSO4·7H2O,洗涤沉淀的基本操作是____________________________________________。
(4)若制得MgSO4·7H2O质量为82.00 g,测得MnO2质量为1.74 g,且测得第①步滤渣质量为4.70 g,忽略各物质在溶液中的溶解损失,可计算出菱镁矿石中MgCO3的质量分数为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在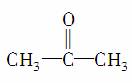 分子中,羰基碳原子与甲基碳原子成键时所采取的杂化方式分别为( )
分子中,羰基碳原子与甲基碳原子成键时所采取的杂化方式分别为( )
A.sp2杂化;sp2杂化 B.sp3杂化;sp3杂化
C.sp2杂化;sp3杂化 D.sp1杂化;sp3杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列变化过程中,原物质分子共价键被破坏,同时还有离子键形成的是( )
A.盐酸和NaOH溶液 B.氯化氢溶于水
C.溴化氢与氨反应 D.锌和稀硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
甲同学认为,在水中加入H2SO4,水的电离平衡向左移动,解释是加入H2SO4后c(H+)增大,平衡左移。乙同学认为,加入H2SO4后,水的电离平衡向右移动,解释为加入H2SO4后,c(H+)浓度增大,H+与OH-中和,平衡右移。你认为哪种说法正确?并说明原因。水的电离平衡移动后,溶液中c(H+)·c(OH-)是增大还是减小?
查看答案和解析>>
科目:高中化学 来源: 题型:
为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2后溶液中Cu2+的含量。实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用Na2S2O3标准溶液滴定至终点。上述过程中发生反应的离子方程式如下:
2Cu2++4I-===2CuI(白色)↓+I2
2S2O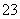 +I2===2I-+S4O
+I2===2I-+S4O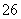
①滴定选用的指示剂为____________,滴定终点观察到的现象为__________________。
②若滴定前溶液中的H2O2没有除尽,所测定的Cu2+含量将会________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能获得成功的是 ( )。
A.将乙醛滴入银氨溶液中,加热煮沸制银镜
B.苯与浓溴水反应制取溴苯
C.向苯酚中加浓溴水观察沉淀
D.1 mol·L-1 CuSO4溶液2 mL和0.5 mol·L-1 NaOH溶液4 mL混合后加入40%的乙醛溶液0.5 mL,加热煮沸观察沉淀的颜色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com