


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题

| A.上下移动①中铜丝可控制SO2的量 |
| B.②中品红溶液不褪色 |
| C.③中石蕊溶液变蓝色 |
| D.为确认CuSO4生成,向①中加水,观察溶液颜色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

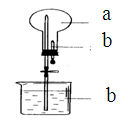
| A.试管中盛酚酞试液,验证氨气的水溶液呈碱性 |
| B.试管中盛酸性高锰酸钾溶液,探究SO2的还原性 |
| C.试管中盛稀氢氧化钠溶液,验证CO2与NaOH反应的产物 |
| D.试管中盛淀粉KI溶液,验证氯气氧化性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
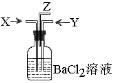
| A.a为HCl,b为H2O |
| B.a为CO2,b为浓NaOH溶液 |
| C.a为Cl2,b为饱和NaCl溶液 |
| D.a为NH3,b为浓NH4Cl溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
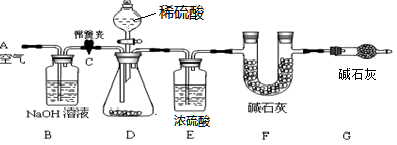
| A.碳跟浓硫酸共热产生的气体X和铜跟浓硝酸反应产生的气体Y |
| B.碳跟浓硫酸共热产生的气体X和铜跟稀硝酸反应产生的气体Y |
| C.MnO2跟浓盐酸共热产生的气体X和碳跟浓硫酸共热产生的气体Y |
| D.碳跟浓硫酸共热产生的气体X和NH4Cl与Ca(OH)2共热产生的气体Y |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.鸡蛋壳发生了分解反应 |
| B.Ⅰ中发生的现象为鸡蛋壳逐渐溶解,产生大量气泡 |
| C.II中的澄清石灰水变浑浊 |
| D.III中紫色石蕊试液变红 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.可以利用烧碱溶液除去混在MgO中的Al2O3 |
| B.用四氯化碳萃取碘水中的碘单质,上层显紫红色 |
| C.将Fe(OH)3沉淀溶于沸水可制得Fe(OH)3胶体 |
| D.测定Na2CO3溶液的pH值,操作时应将先pH试纸润湿 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.银镜反应实验后附有银的试管,可用稀H2SO4清洗 |
| B.在中学《硫酸铜晶体里结晶水含量测定》的实验,称量操作至少需要四次 |
| C.不慎将浓H2SO4沾在皮肤上,立即用NaOH溶液冲洗 |
| D.在250ml 烧杯中,加入216g水和24g NaOH固体,配制10% NaOH溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com