
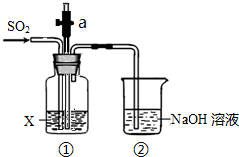
 某实验小组用如图所示装置探究SO2的性质.
某实验小组用如图所示装置探究SO2的性质.分析 (1)二氧化硫是污染性气体,不能排放到空气中,需要用氢氧化钠溶液吸收;
(2)二氧化硫具有漂白性,可以使品红溶液褪色;
(3)二氧化硫通入紫色石蕊试液生成亚硫酸显示酸性;
(4)高锰酸钾溶液具有强氧化性,二氧化硫具有还原性,二者发生氧化还原反应;
(5)二氧化硫排放会形成酸雨污染环境;
解答 解:(1)二氧化硫是污染性气体,不能排放到空气中,需要用氢氧化钠溶液吸收,装置②在实验中的作用是:尾气吸收,防止污染空气,
故答案为:尾气吸收,防止污染空气;
(2)二氧化硫具有漂白性,可以使品红溶液褪色,若X为品红溶液,可观察到装置①中溶液褪色,说明SO2具有漂白性,
故答案为:漂白性;
(3)二氧化硫通入紫色石蕊试液生成亚硫酸显示酸性,若X为紫色石蕊溶液,可观察到装置①中溶液变红,说明SO2的水溶液显酸性,选a,
故答案为:a;
(4)高锰酸钾溶液具有强氧化性,二氧化硫具有还原性,二者发生氧化还原反应,若X为紫红色酸性高锰酸钾溶液(强氧化剂),可观察到装置①中溶液颜色变浅或褪色.SO2在该实验中表现还原性,
故答案为:还原;
(5)二氧化硫排放会污染环境,若空气中排放的SO2超量,则引起的环境问题将会是形成酸雨,
故答案为:酸雨;
点评 本题考查了二氧化硫的性质实验验证、反应现象的判断,掌握基础是解题关键,题目难度不大.


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源:2017届江苏省如皋市高三上学期质量调研一化学试卷(解析版) 题型:计算题
黄钠铁矾[NaaFeb(SO4)c(OH)d]具有沉淀颗粒大、沉淀速率快、容易过滤等特点。某研究小组先将某废水中Fe2+氧化为Fe3+,再加入Na2SO4使其生成黄钠铁矾而除去铁。为测定黄钠铁矾的组成,该小组进行了如下实验:
①称取12.125 g样品,加盐酸完全溶解后,配成250.00 mL溶液A。
②量取25.00 mL溶液A,加入足量的KI,再用0.2500 mol·L-1 Na2S2O3溶液滴定生成的I2(反应原理为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00 mL Na2S2O3溶液至终点。
③另取50.00 mL溶液A,加入足量BaCl2溶液充分反应后,过滤,将所得沉淀洗涤、干燥后,称得其质量为2.330 g。
(1)NaaFeb(SO4)c(OH)d中a、b、c、d之间的代数关系式为 。
(2)通过计算确定黄钠铁矾的化学式(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
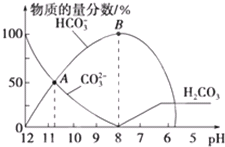
| A. | 当溶液的pH=7时,溶液的总体积为20mL(若忽略溶液混合后体积的变化) | |
| B. | 在0.1mol/L 的Na2CO3溶液中:c(Na+)+c(H+)═c(CO32-)+c(OH-)+c(HCO3-) | |
| C. | 在A点所示的溶液中:c(CO32-)═c(HCO3-)>c(H+)>c(OH-) | |
| D. | 在B点所示的溶液中,浓度最大的阳离子是Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为94、中子数为144的钚(Pu)原子:14494Pu | |
| B. | H2O2的电子式: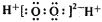 | |
| C. | S2-离子结构示意图: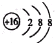 | |
| D. | 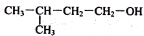 的名称2-甲基-4-丁醇 的名称2-甲基-4-丁醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
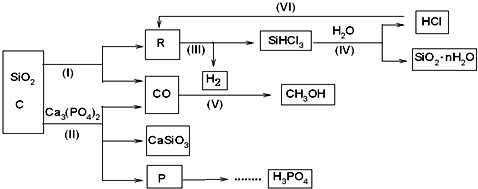
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl | B. | NaNO2 | C. | NaNO3 | D. | BaSO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com