
 Ęū³µĪ²Ęų¾»»ÆµÄÖ÷ŅŖŌĄķĪŖ£ŗ2NO£Øg£©+2CO£Øg£©?2CO2£Øg£©+N2£Øg£©”÷H£¼0
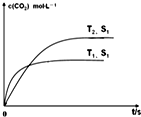
Ęū³µĪ²Ęų¾»»ÆµÄÖ÷ŅŖŌĄķĪŖ£ŗ2NO£Øg£©+2CO£Øg£©?2CO2£Øg£©+N2£Øg£©”÷H£¼0·ÖĪö ÉżøßĪĀ¶Č£¬»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£¬»ÆŃ§Ę½ŗāĻņ×ÅĪüČČ·½ĻņŅĘ¶Æ£¬Ōö¼Ó“߻ƼĮµÄ±ķĆ껿£¬·“Ó¦ĖŁĀŹ¼Óæģ£¬µ«ŹĒ²»»įŅżĘš»ÆŃ§Ę½ŗāµÄøı䣮
½ā“š ½ā£ŗøł¾ŻĶ¼Ź¾£¬ÉżøßĪĀ¶Č£¬»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£¬ĻČ¹ÕĻČĘ½·“Ó¦æģ£¬ĖłŅŌT1£¾T2£¬½µµĶĪĀ¶Č£¬Ę½ŗā»įÕżĻņŅĘ¶Æ£¬ĖłŅŌ¶žŃõ»ÆĢ¼µĆÅضČŌö“󣻓߻ƼĮµÄ±ķĆ껿S1£¾S2£¬Ōö¼Ó“߻ƼĮµÄ±ķĆ껿£¬·“Ó¦ĖŁĀŹ¼Óæģ£¬µ«ŹĒ²»»įŅżĘš»ÆŃ§Ę½ŗāµÄøı䣬ĖłŅŌŗĶT2”¢S1ĻĀ½ØĮ¢µÄĘ½ŗāŹĒŅ»ŃłµÄ£¬ĖŁĀŹ»į¼õĀż£¬¹Ź“š°øĪŖ£ŗ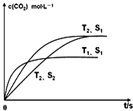 £®
£®
µćĘĄ ±¾Ģāæ¼²éѧɜ»Æѧ·“Ó¦ĖŁĀŹŗĶĘ½ŗāŅĘ¶ÆµÄÓ°ĻģŅņĖŲÖŖŹ¶£¬×¢ŅāÖŖŹ¶µÄ¹éÄÉŗĶŹįĄķŹĒ¹Ų¼ü£¬ÄѶČÖŠµČ£®


 øߊ§ÖĒÄÜæĪŹ±×÷ŅµĻµĮŠ“š°ø
øߊ§ÖĒÄÜæĪŹ±×÷ŅµĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CO2 | B£® | ŃĪĖį | C£® | CaCO3 | D£® | NaOHČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³ĘČ”8.0 gĮņĖįĶ¹ĢĢ壬¼ÓČė500 mLĖ® | |
| B£® | ÅäÖĘŗƵÄĮņĖįĶČÜŅŗÓ¦×ŖŅʵ½ĻøæŚŹŌ¼ĮĘæÖŠ£¬²¢ĢłÉĻ±źĒ© | |
| C£® | µĪ¼ÓÕōĮóĖ®²»É÷³¬¹żæĢ¶ČĻߣ¬Į¢¼“ÓĆ½ŗĶ·µĪ¹Ü½«¶ąÓąµÄŅŗĢåĪü×ß | |
| D£® | ¶ØČŻŅ”ŌČŗ󣬷¢ĻÖÅäÖĘČÜŅŗŅŗĆęµĶÓŚæĢ¶ČĻߣ¬Ó¦ÓĆ½ŗĶ·µĪ¹ÜµĪ¼ÓÕōĮóĖ®ÖĮæĢ¶ČĻß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | X£¾Z£¾Y£¾M | B£® | X£¾Y£¾Z£¾M | C£® | M£¾Z£¾X£¾Y | D£® | X£¾Z£¾M£¾Y |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ķ¬ĻµĪļ | B£® | Ķ¬Ī»ĖŲ | C£® | Ķ¬ÖÖĪļÖŹ | D£® | Ķ¬·ÖŅģ¹¹Ģå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com