
| A. | A、B两种元素可组成化学式为BA4的化合物 | |
| B. | F与D形成的化合物性质很不活泼,不与任何酸反应 | |
| C. | 原子半径由大到小的顺序是C>B | |
| D. | 气态氢化物的稳定性由强到弱的顺序是C>D |
分析 六种短周期元素A、B、C、D、E、F的原子序数依次增大,单质F是一种重要的半导体材料,则F为Si元素;B与F同主族,则B为C元素;已知A与其他元素不在同一周期,则A处于第一周期,为H元素;E的原子序数大于B,则E为Na元素;D的核电荷数是B的最外层电子数的2倍,则D的核电荷数为8,是O元素;结合原子序数可知C只能为N元素,据此进行解答.
解答 解:六种短周期元素A、B、C、D、E、F的原子序数依次增大,单质F是一种重要的半导体材料,则F为Si元素;B与F同主族,则B为C元素;已知A与其他元素不在同一周期,则A处于第一周期,为H元素;E的原子序数大于B,则E为Na元素;D的核电荷数是B的最外层电子数的2倍,则D的核电荷数为8,是O元素;结合原子序数可知C只能为N元素,
A.A、B分别为H、C元素,二者可以形成化学式为CH4的化合物,故A正确;
B.F与D形成的化合物为二氧化硅,二氧化硅的性质很不活泼,一般不与强酸反应,但可以与氢氟酸发生反应,故B错误;
C.B、C处于同一周期,原子序数越大,其原子半径越小,则原子半径大小为:B>C,故C错误;
D.非金属性越强,气态氢化物的稳定性越强,非金属性O>N,则气态氢化物的稳定性:C<D,故D错误;
故选A.
点评 本题考查了原子结构与元素周期律的应用,题目难度中等,涉及原子半径大小比较、二氧化硅的性质、气态氢化物的稳定性等知识,推断元素为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:解答题
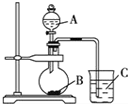 某研究性学习小组设计了一组实验验证非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强.他们设计了如图装置以验证 氮、碳、硅元素的非金属性强弱.他们设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成.
某研究性学习小组设计了一组实验验证非金属元素的非金属性越强,对应的最高价含氧酸的酸性就越强.他们设计了如图装置以验证 氮、碳、硅元素的非金属性强弱.他们设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
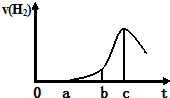 某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500mL 0.5mol•L-1的硫酸溶液中,下图为反应产生氢气速率与反应时间的关系图.
某兴趣小组进行“活泼金属与酸反应”的实验,将5.4g的铝片投入500mL 0.5mol•L-1的硫酸溶液中,下图为反应产生氢气速率与反应时间的关系图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到上层液体呈紫色 | |
| B. | 液溴有强挥发性,保存时应加少量水液封 | |
| C. | Cl2可以从NaBr水溶液中置换出溴单质,可类推F2可以从NaCl水溶液中置换出氯单质 | |
| D. | HX的还原性顺序为:HF>HCl>HBr>HI |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 10%H2O2的体积/mL | 5.0 | 5.0 | v1 | v2 |
| 20%硫酸的体积/mL | 0 | 0.5 | 1.0 | v3 |
| 水的体积/mL | 15 | 14.5 | v4 | 13.5 |
| 所需时间/min | t1 | t2 | t3 | t4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
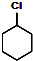 $→_{②}^{NaOH,乙醇,△}$
$→_{②}^{NaOH,乙醇,△}$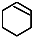 $→_{③}^{Br_{2}的CCl_{4}溶液}$B$\stackrel{④}{→}$
$→_{③}^{Br_{2}的CCl_{4}溶液}$B$\stackrel{④}{→}$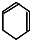
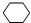 ,B的结构简式是
,B的结构简式是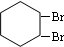 ;
; .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com